题目内容
镁一过氧化氢燃料电池具有比能量高、安全方便等优点,其总反应为Mg+H2O2+H2SO4=MgSO4+2H2O,结构示意图如图所示。下列关于该电池的叙述正确的是
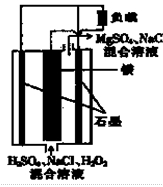
A.电池内部可以使用MnO2作填料
B.电流工作时,H+向Mg电极移动
C电池工作时,正极的电板反应式为Mg—2e— Mg2+
D.电池工作时,电解质溶液的pH将不断变大

A.电池内部可以使用MnO2作填料
B.电流工作时,H+向Mg电极移动
C电池工作时,正极的电板反应式为Mg—2e—
D.电池工作时,电解质溶液的pH将不断变大
D
试题分析:A、根据总反应:Mg+H2O2+H2SO4═MgSO4+2H2O可知电池中有双氧水,加入MnO2作填料,能使双氧水加速分解,所以不能用MnO2作填料,故错误; B、电流工作时,H+向正极移动,Mg失电子为负极,故B错误; C、根据总反应:Mg+H2O2+H2SO4═MgSO4+2H2O,则负极是金属镁发生失电子的氧化反应,即Mg-2e-═Mg2+,故错误; D、根据总反应:Mg+H2O2+H2SO4═MgSO4+2H2O,电池工作时,消耗硫酸,溶液中氢离子浓度减小,所以电解质溶液的pH将不断变大,故正确.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
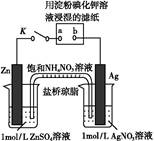
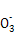 向Zn电极移动
向Zn电极移动
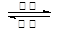 2CO32- + 6H2O,则下列说法正确的是
2CO32- + 6H2O,则下列说法正确的是