题目内容
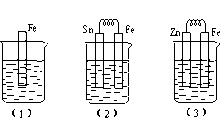
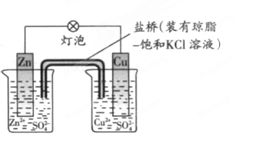
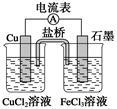
关于下列装置说法正确的是
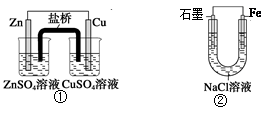

| A.装置①中,盐桥中的K+移向CuSO4溶液 |
| B.装置①中,Zn为负极,发生还原反应 |
| C.装置②中的Fe发生析氢腐蚀 |
| D.装置②中电子由Fe流向石墨,然后再经溶液流向Fe |
A
试题分析:A.装置①为原电池反应。Zn作负极,Cu作正极。根据同种电荷相互排斥,异种电荷相互吸引的原则,盐桥中的K+移向负电荷较多的正极一方,即盛有CuSO4溶液的烧杯中。正确。B.装置①中,Zn为负极,发生氧化反应Zn-2e-=Zn2+。错误。C.在装置②的原电池反应中。由于NaCl溶液是中性溶液,所以其中的Fe发生的是吸氧腐蚀。错误。D.活动性Fe大于C,所以Fe失去电子,作负极,电子经导线流向石墨,然后在正极C上发生还原反应O2+4e-+2H2O=4OH-。在溶液中,Na+向C电极移动,Cl-向Fe电极移动。形成闭合回路。错误。

练习册系列答案
相关题目