题目内容
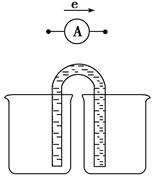
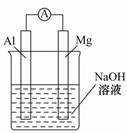
将镁条、铝条平行插入盛有一定浓度的NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示。此电池工作时,下列叙述正确的是( )

| A.Mg比Al活泼,Mg失去电子被氧化成Mg2+ |
| B.铝条表面虽有氧化膜,但可不必处理 |
| C.该电池的内外电路中,电流均是由电子定向移动形成的 |
| D.Al是电池负极,开始工作时溶液中会立即有白色沉淀析出 |
B
本题是新情境下原电池的相关试题,解题的关键仍然是要明确原电池工作时所对应的自发氧化还原反应,在碱性条件下,金属镁不能发生反应,而单质Al则能与NaOH反应生成NaAlO2和H2,则Al为还原剂,作原电池负极。A项,电解质溶液为NaOH溶液,Al失电子,为负极,错。B项,铝条表面的氧化膜为Al2O3,Al2O3能与NaOH溶液反应,故不必处理,对。C项,在内电路中电流是阴、阳离子定向移动形成的,错。D项,电池工作时铝元素的反应为Al→AlO2-,所以无沉淀产生,错

练习册系列答案
相关题目