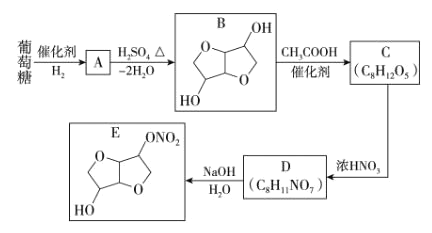
题目内容
【题目】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示。则该元素对应的原子有___种不同运动状态的电子。
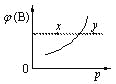
(2)如图2所示.每条折线表示周期表IVA–VIIA中的某一族元素氢化物的沸点变化。请解释AsH3比NH3沸点低的原因___。
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该CO2晶体属于___晶体。

(4)第一电离能介于Al、P之间的第三周期元素有__种。BCl3中B原子的杂化方式为___。
(5)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的A-D图示中正确的是__(填字母标号)。

铁原子的配位数是___,假设铁原子的半径是rcm,该晶体的密度是ρg/cm3,则铁的相对原子质量为___(设阿伏加德罗常数的值为NA)。
【答案】12 NH3存在分子间氢键 原子 3 sp2杂化 A 8 ![]()
【解析】
(1)根据电离能产生的突变得到最外层电子数,得到元素名称;
(2)根据晶体类型和晶体中粒子间作用力分析;
(3)根据晶胞特点分析;
(4)同周期主族元素从左到右第一电离能呈增大趋势,但第ⅡA族最外能层的s能级全满,处于稳定状态,第ⅤA族最外能层的p能级半充满,较稳定;根据杂化轨道理论求杂化类型;
(5)相对原子质量的计算利用密度公式进行。
(1)第三周期的某主族元素,根据第一至第五电离能数据,可知,该原子第二和第三电离能变化较大,产生了突变,则该原子最外层有2个电子,为镁元素,其核外有12个电子,每个电子的运动状态都不同,则有12种不同运动状态的电子;
(2) NH3分子间能形成氢键,而AsH3分子间无氢键,所以AsH3比NH3沸点低;
(3) 由CO2在高温高压下所形成的晶体的晶胞图可知,在晶胞中原子之间通过共价键结合形成空间网状结构的晶体,属于原子晶体;
(4)同周期主族元素从左到右第一电离能呈增大趋势,但第ⅡA族最外能层的s能级全满,处于稳定状态,第ⅤA族最外能层的p能级半充满,较稳定,故第三周期元素的第一电离能由大到小的顺序为Na<Al<Mg<Si<S<P<Cl<Ar,所以第一电离能介于Al、P之间的第三周期元素有3种;BCl3中B原子无孤电子对,成键电子对数为3,B的杂化方式为sp2杂化;
(5) 图甲中Fe位于顶点和体心,乙由8个甲组成,按虚线方向切乙形成的截面边长不等,排除B、D,由于每个小立方体的体心有一个铁原子,故A正确;由图甲可以看出,位于体心的铁原子周围距离最近的铁原子有8个,所以铁原子的配位数是8;
因为铁原子的半径是r cm,根据铁晶胞的结构可知,晶胞的边长为![]() ,在每个晶胞中含有铁原子的数目为1+8×
,在每个晶胞中含有铁原子的数目为1+8×![]() =2,设铁原子相对原子质量为M,根据密度=质量除以体积,可得ρ=
=2,设铁原子相对原子质量为M,根据密度=质量除以体积,可得ρ=![]() ,所以M=
,所以M=![]() 。
。

 名校课堂系列答案
名校课堂系列答案【题目】某学生探究如下实验(A):
实验A | 条件 | 现象 |
| 加热 | i.加热后蓝色褪去 ii.冷却过程中,溶液恢复蓝色 ⅲ.一段时间后,蓝色重又褪去 |
(1)使淀粉变蓝的物质是____。
(2)分析现象i、ii认为:在酸性条件下,加热促进淀粉水解,冷却后平衡逆向移动。
设计实验如下,“现象a”证实该分析不合理:

“现象a”是____。
(3)再次分析:加热后单质碘发生了变化,实验如下:
I:取少量碘水,加热至褪色,用淀粉溶液检验挥发出的物质,变蓝。
Ⅱ:向褪色后的溶液中滴加淀粉溶液,冷却过程中一直未变蓝;加入稀H2SO4,瞬间变蓝。
对步骤Ⅱ中稀H2SO4的作用,结合离子方程式,提出一种合理的解释:______________。
(4)探究碘水褪色后溶液的成分:
实验1:测得溶液的pH≈5
实验2:取褪色后的溶液,完成如下实验:

①产生黄色沉淀的离子方程式是____。
②Ag2O的作用是____________。
③依据上述实验,推测滤液中含有的物质(或离子)可能是_________。
(5)结合化学反应速率解释实验A中现象i、现象iii蓝色褪去的原因:_______________。