题目内容
【题目】下列有关电化学装置的叙述正确的是

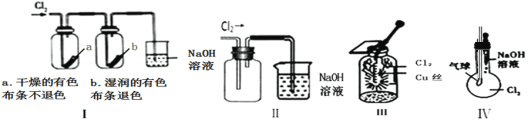
A.图1中,Zn—MnO2干电池放电时,MnO2被氧化
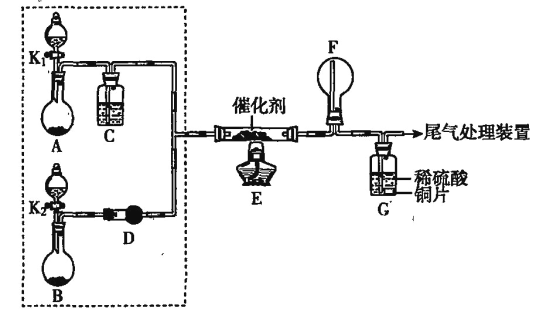
B.图2中,电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等
C.图3中,K分别与M、N连接,均可保护Fe电极,连接M时称为“牺牲阳极的阴极保护法”
D.图4中,在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl7-形式存在,则阳极反应式为:Al -3e-+7AlCl4-= 4Al2Cl7-
【答案】D
【解析】
A、锌作原电池的负极,发生氧化反应,被氧化,而不是MnO2被氧化,故A错误;
B、电解精炼时,粗铜作阳极,纯铜作阴极,而粗铜中有比铜活泼的金属比如Fe、Zn,先放电,而阴极一直是Cu2+得到电子生成Cu,所以阳极减少的质量与阴极增加的质量不相等,故B错误;
C、K与M相连接,铁作阴极,受保护;而K与N相连接,构成原电池,铁电极为正极,受保护,称为"牺牲阳极的阴极保护法”,所以前者是外接电流的阴极保护法,故C错误;
D、铝与电源的正极相连,作阳极,阳极发生氧化反应,所以电极反应式为::Al -3e-+7AlCl4-= 4Al2Cl7-,故D正确;
故选D。

练习册系列答案
相关题目