题目内容
正确掌握化学用语是学好化学的基础,下列有关表述正确的是( )
| A、H、D、T互为同素异形体 |
| B、氨分子中的化学键为非极性共价键 |
C、NH4Cl的电子式: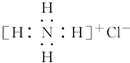 |
D、S2-的结构示意图: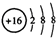 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.同素异形体为同种元素的不同单质,研究对象为单质;
B.氨气分子中存在3个N-H键,氮氢键为极性共价键;
C.氯化铵为离子化合物的,氯离子没有标出最外层电子;
D.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构.
B.氨气分子中存在3个N-H键,氮氢键为极性共价键;
C.氯化铵为离子化合物的,氯离子没有标出最外层电子;
D.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构.
解答:
解:A.H、D、T为氢元素的不同原子,互为同位素,不属于同分异构体,故A错误;
B.氨气分子中的化学键为N-H键,属于极性共价键,氨气分子中不存在非极性共价键,故B错误;
C.氯化铵中存在铵根离子和氯离子,电子式中既要标出离子所带电荷,还要标出最外层电子,氯化铵正确的电子式为: ,负C错误;
,负C错误;
D.硫离子核电荷数为16,最外层为8个电子,硫离子的结构示意图为: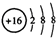 ,故D正确;
,故D正确;
故选D.
B.氨气分子中的化学键为N-H键,属于极性共价键,氨气分子中不存在非极性共价键,故B错误;
C.氯化铵中存在铵根离子和氯离子,电子式中既要标出离子所带电荷,还要标出最外层电子,氯化铵正确的电子式为:
 ,负C错误;
,负C错误;D.硫离子核电荷数为16,最外层为8个电子,硫离子的结构示意图为:
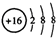 ,故D正确;
,故D正确;故选D.
点评:本题考查了电子式、离子结构示意图、共价键的类型、同素异形体与同位素的判断,题目难度中等,注意掌握常见化学用语的概念及正确的表示方法,明确同位素与同系物、同素异形体的区别,明确离子化合物与共价化合物的电子式的正确表示方法.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
据报道N5是破坏力极强的炸药之一,18O2比黄金还贵重的物质.下列说法正确的是( )
| A、18O2中含18个中子 |
| B、18O2与16O2性质完全相同 |
| C、N5和N2互为同位素 |
| D、2N5═5N2是化学变化 |
下列物质中不属于合金的是( )
| A、不锈钢 | B、白铜 |
| C、高碳钢 | D、金刚石 |
下列反应中硝酸既表现氧化性,又表现酸性的是( )
| A、氧化铝和硝酸 |
| B、氧化铜和硝酸 |
| C、硫化氢和硝酸 |
| D、铜和浓硝酸 |
下列比较或归纳正确的是( )
| A、稳定性:NH3<PH3<ASH3 |
| B、离子半径:Cl->S2->Al3+ |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:Be(OH)2>Mg(OH)2>Al(OH)3 |
根据酸碱质子理论判定下列说法不正确的是( )
| A、所有的弱酸根都是碱 |
| B、酸式弱酸根既是酸又是碱 |
| C、不可能一种物质既是酸又是碱 |
| D、氢氧根是碱 |
下列叙说正确的是( )
| A、一定温度下,若等浓度的NaA,NaB溶液,pH前者大于后者,则HA,HB的Ka前者小于后者 |
| B、在一定温度下的CaSO4的水溶液中,Ca2+和SO42-浓度的乘积是一定是常数 |
| C、常温时,浓度均为0.01mol/L Na2CO3溶液和NaHCO3溶液,等体积混合,其溶液中粒子浓度关系为3c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3) |
D、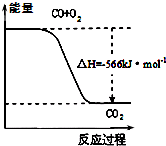 已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ?mol-1图可表示由CO生成CO2的反应过程和能量关系 |
下列说法正确的是( )
| A、不含其他杂质的天然油脂属于纯净物 |
| B、油脂在酸性或碱性条件下都比在纯水中易水解 |
| C、各种油脂水解后的产物中都有甘油 |
| D、油脂的烃基部分饱和程度越大,熔点越低 |