题目内容
14.下列实验事实与图象对应正确的是( )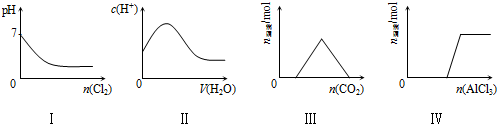
| A. | I表示向Na2SO3溶液中通入Cl2 | |
| B. | II表示向纯CH3COOH中逐滴加水并不断振荡 | |
| C. | III表示向KOH和Ca(OH)2混合液中通入CO2 | |
| D. | Ⅳ表示向NaOH溶液中逐滴加入AlCl3溶液并不断振荡 |
分析 A、Na2SO3溶液显碱性;
B、纯醋酸不电离,不存在氢离子;
C、向KOH和Ca(OH)2混合液中通入CO2,开始就生成沉淀;
D、向NaOH溶液中逐滴加入AlCl3溶液,开始生成Na[Al(OH)4],NaOH反应完全后,Na[Al(OH)4]再与AlCl3反应生成Al(OH)3沉淀.
解答 解:A、Na2SO3溶液显碱性,通入氯气之前,其pH应大于7,故A错误;
B、纯CH3COOH中氢离子浓度为0,故B错误;
C、二氧化碳与氢氧根离子反应生成碳酸根离子,与钙离子反应生成沉淀,生成沉淀应从0点开始产生沉淀,故C错误;
D、向NaOH溶液中逐滴加入AlCl3溶液,开始生成Na[Al(OH)4],NaOH反应完全后,Na[Al(OH)4]再与AlCl3反应生成Al(OH)3沉淀,与图象相符合,故D正确;
故选D.
点评 本题通过图象分析考查了盐类水解、弱酸的电离、离子反应的实质、氢氧化铝的两性,题目难度较大.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | 加热NH4C1晶体时,将湿润的红色石蕊试纸靠近试管口,检验NH3的生成 | |
| B. | 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ | |
| C. | 除去KNO3中的少量NaCl,可将混合物制成热的饱和溶液,冷却结晶,过滤 | |
| D. | 通过灼热的镁粉除去N2中的O2 |
5.下列各组离子一定能大量共存的是( )
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在使酚酞变红的溶液中:Na+、K+、AlO2-、CO32- | |
| C. | 在水电离产生的c(OH-)=1×10-14mol•L-1的溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 在pH试纸变深红色的溶液中:K+、Fe2+、Cl-、NO3- |
2.在25℃时,浓度均为0.2mol/L的NaHCO3和Na2CO3溶液中,下列判断正确的是( )
| A. | c(OH-)前者大于后者 | |
| B. | 与同浓度的盐酸反应时的反应速率前者大于后者 | |
| C. | 分别加入1L的0.2 mol/L的HNO3 后一定产生4.48LCO2 | |
| D. | 溶液中阳离子浓度相同 |
9.已知:
①2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol;
②H2(g)+S(g)═H2S(g)△H=-20.1kJ/mol.
下列判断一定正确的是( )
①2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol;
②H2(g)+S(g)═H2S(g)△H=-20.1kJ/mol.
下列判断一定正确的是( )
| A. | 由①知,氢气的燃烧热为241.8 kJ | |
| B. | 由①、②知,2H2S(g)+O2(g)=2S(g)+2H2O(g)△H=-443.4kJ/mol | |
| C. |  反应②中的能量变化可用如图表示 | |
| D. | 若反应②中改用固态硫,则放热大于20.1 kJ |
3.根据下列实验事实判断所测液体样品最有可能是纯水的是( )
| A. | 室温下测定其pH等于7 | |
| B. | 一个标准大气压下测定其沸点为100℃ | |
| C. | 电解时产生H2、O2的体积比为2:1 | |
| D. | 室温时为无色的液体 |
18.著名化学家徐光宪获得国家最高科学技术奖,以表彰他在稀土萃取理论方面作出的贡献.已知:金属铈(稀土元素)在空气中易氧化变暗,受热时燃烧,遇水很快反应.(注:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2.)下列说法正确的是( )
| A. | 铈溶于氢碘酸的化学方程式可表示为:Ce+4HI $\frac{\underline{\;高温\;}}{\;}$ CeI4+2H2↑ | |
| B. | 用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+═Ce3++2Fe3+ | |
| C. | 金属Ce保存时,应该隔绝空气和水 | |
| D. | 铈的四种核素136 58Ce、138 58Ce、140 58Ce、142 58Ce,它们互称为同素异形体 |
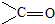 )的化合物反应生成醇:
)的化合物反应生成醇: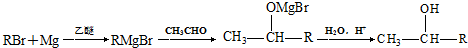


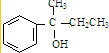 ,F
,F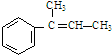 ,G
,G .
. $\stackrel{AlCl_{3}}{→}$
$\stackrel{AlCl_{3}}{→}$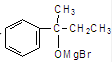 .
. ;若E′与浓硫酸共热不能得到碳链不变的烯烃,则E′可能的结构简式为
;若E′与浓硫酸共热不能得到碳链不变的烯烃,则E′可能的结构简式为 .
.