题目内容
2.下列粒子的结构示意图中,表示氯离子的是( )| A. | 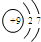 | B. | 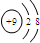 | C. | 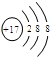 | D. |  |
分析 当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子.
解答 解:A、质子数为9,核外电子数为8,表示氟原子,故A不符合;
B、质子数为9,核外电子数为10,表示氟离子,故B不符合;
C、质子数为17,核外电子数为18,表示氯离子,故C符合;
D、质子数为17,核外电子数为17,表示氯原子,故D不符合;
故选C.
点评 本题主要考查对原子结构示意图,离子结构示意图等考点的理解,难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
12.现有反应S2Cl2(l)(橙黄色)+Cl2(g)?2SCl2(l)(鲜红色)△H=-50.16kJ•mol-1.在密闭容器中达到平衡,下列说法错误的是( )
| A. | 温度不变,增大容器的体积,S2Cl2的转化率降低 | |
| B. | 温度不变,缩小容器体积,液体的颜色加深 | |
| C. | 压强不变,升高温度,液体的颜色变浅 | |
| D. | 体积不变,降低温度,氯气的转化率降低 |
13.200mL 0.3mol/L Na2SO4溶液和100mL 0.2mol/L Al2(SO4)3的溶液混合后,加水稀释至500mL.稀释后溶液中SO42-的物质的量的浓度为( )
| A. | 0.4mol/L | B. | 0.24mol/L | C. | 0.35mol/L | D. | 0.5mol/L |
10.用18O标记的叔丁醇[(CH3)3C-18OH]与乙酸发生酯化反应(记为反应①)、用18O标记的乙醇(C2H5-18OH)与硝酸发生酯化反应(记为反应②)后,18O都存在于水中.关于上述两个反应机理有这样两个解释:
Ⅰ、酸提供羟基、醇提供羟基上的氢原子结合成水;
Ⅱ、醇提供羟基、酸提供羟基上的氢原子结合成水.
下列叙述中正确的是( )
Ⅰ、酸提供羟基、醇提供羟基上的氢原子结合成水;
Ⅱ、醇提供羟基、酸提供羟基上的氢原子结合成水.
下列叙述中正确的是( )
| A. | ①、②两个反应的机理都是Ⅰ | B. | ①、②两个反应的机理都是Ⅱ | ||
| C. | ①的机理是Ⅰ,②的机理是Ⅱ | D. | ①的机理是Ⅱ,②的机理是Ⅰ |
7.最近科学家成功制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述正确的是( )
| A. | 该晶体的熔沸点低、硬度小 | |
| B. | 晶体中碳原子数与C-O化学键数之比为1:2 | |
| C. | 晶体的空间最小环共有6个原子构成 | |
| D. | 该晶体中碳原子和氧原子的个数比为1:2 |
7.关于盐类水解,下列叙述不正确的是( )
| A. | 是中和反应的逆反应 | |
| B. | 水的电离平衡被破坏 | |
| C. | 盐类水解破坏盐的电离平衡 | |
| D. | 配制硫酸铜溶液时,加入适量的硫酸,是为了抑制硫酸铜的水解 |
4.一定温度下,向一个容积为2L的真空密闭容器中(事先装入催化剂)通入1mol N2和3mol H2,发生下列反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3.3min后测得密闭容器内的压强是起始时的0.9倍,在此时间内v(H2)是( )
| A. | 0.2 mol/(L•min) | B. | 0.6 mol/(L•min) | C. | 0.1 mol/(L•min) | D. | 0.3 mol/(L•min) |
5.下列实验可实现鉴别目的是( )
| A. | 用BaCl2溶液鉴别SO3(g)和SO2 | |
| B. | 用Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液 | |
| C. | 用CO2鉴别Na[Al(OH)4]溶液和Na2SiO3溶液 | |
| D. | 用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2 |