题目内容
【题目】CO、H2、CH3OH均是清洁能源。
(1)已知部分化学键键能数据如下:
化学键 | C | O=O | C=O | C-O |
E/(kJ mol-1) | 958.5 | 497 | 745 | 351 |
2CO(g) +O2(g)==2CO2(g) ![]() H1 H2O(g)+CO(g)==H2(g) + CO2(g)
H1 H2O(g)+CO(g)==H2(g) + CO2(g) ![]() H2 = -41 kJmol-1
H2 = -41 kJmol-1
CH3OH(g)+ 3/2O2(g)==CO2(g)+2H2O(g) ![]() H3 = -660kJmol-1
H3 = -660kJmol-1
则△H1=_____ kJmol-1,反应CO(g)+2H2(g)![]() CH3OH(g)的△H=_____ kJmol-1。
CH3OH(g)的△H=_____ kJmol-1。
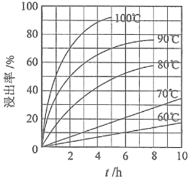
(2)一定条件下,在容积为2 L的密闭容器Q中充入a mol CO与b molH2合成甲醇:CO(g) +2H2(g) ![]() CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。
CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。

①压强相同时,温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者之间的相对大小为t1___ t2(填“>”、“<”、“=”或“无法确定”)。
②P1_____P2(填“>”、“<”、“=”或“无法确定”)。
③若a =2,b=4,则压强为P1、温度为T1时该反应的平衡常数K=______________。
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体,则反应开始时,v(CH3OH)正_____v(CH3OH)逆(填“>”、“<”、“=”或“无法确定”)。
【答案】-566 -107 > > 4.5 无法确定
【解析】
(1)根据化学方程式及化学键键能数据,![]() H1
H1![]() ;根据盖茨定律,CO(g)+2H2(g)
;根据盖茨定律,CO(g)+2H2(g)![]() CH3OH(g)的
CH3OH(g)的 ,故本小题答案为:-566;-107;
,故本小题答案为:-566;-107;
(2)①因为CO(g) +2H2(g)![]() CH3OH(g) △H=-107kJmol-1,所以温度越高,平衡时CH3OH的含量越低,所以图1中T2>T1,压强相同、温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者的相对大小关系为t1>t2,本小题的答案为:>;
CH3OH(g) △H=-107kJmol-1,所以温度越高,平衡时CH3OH的含量越低,所以图1中T2>T1,压强相同、温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者的相对大小关系为t1>t2,本小题的答案为:>;
②已知a mol CO与b molH2合成甲醇,故投料物质的量之比(用X表示)为:![]() ;由图2知,投料比相同时,压强为P1时氢气平衡转化率高,又因为该反应正向为气体体积减小的反应,故P1>P2,本小题答案为:>;
;由图2知,投料比相同时,压强为P1时氢气平衡转化率高,又因为该反应正向为气体体积减小的反应,故P1>P2,本小题答案为:>;
③若a=2,b=4,则压强为P1、温度为T1时,列三段式:
CO(g) +2H2(g)![]() CH3OH(g)
CH3OH(g)
开始(mol)2 4 0
转化(mol)x 2x x
平衡(mol)2-x 4-2x x
由图1,此条件下平衡时CH3OH的体积分数为40%,所以:![]() ,解得
,解得![]() ,所以平衡时n(CO)=
,所以平衡时n(CO)=![]() mol,n(H2)=
mol,n(H2)=![]() mol,又因为容积为2L,所以CO、H2、CH3OH的平衡浓度分别为:
mol,又因为容积为2L,所以CO、H2、CH3OH的平衡浓度分别为:![]() mol·L-1、
mol·L-1、![]() mol·L-1、
mol·L-1、![]() mol·L-1,故
mol·L-1,故![]() ,本小题答案为:4.5;
,本小题答案为:4.5;
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体(设为y),此时浓度商=![]() ,与K无法比较大小,不能确定平衡向哪个方向移动,故无法确定ν(CH3OH)正与ν(CH3OH)逆的大小。
,与K无法比较大小,不能确定平衡向哪个方向移动,故无法确定ν(CH3OH)正与ν(CH3OH)逆的大小。

【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50 s的平均速率为v(PCl3)=0.0032mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%