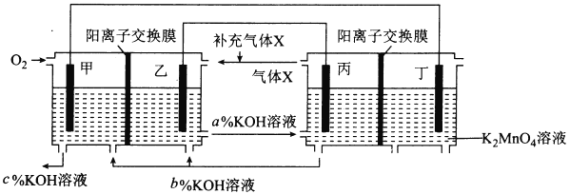
题目内容
【题目】实验室中H2SO4、NaOH是两种常见试剂。
(1)现在实验室中有一瓶98%的H2SO4(ρ=1.84g/cm3)。
①该硫酸的物质的量浓度为____________mol/L;
②现要配置2.0mol/L的稀H2SO4250mL,请回答如下问题:需要量取浓硫酸的体积为________(保留一位小数).在该实验使用的玻璃仪器中除烧杯、玻璃棒、胶头滴管、量筒外,还有__________。
(2)有一瓶氢氧化钠固体由于放置时间较长,某同学怀疑其由于吸收空气中CO2而发生部分变质。为证明此推测,进行如下实验。
称取2.000g样品,配制成250mL待测液。量取20.00mL待测液,当慢慢滴入0.100mol/L的硫酸溶液18.60mL时测得溶液正好显中性.根据实验数据可知:
待测溶液中氢氧化钠的浓度为_____________mol/L;
样品中氢氧化钠的质量百分数为______________。
由此,该同学得出结论:样品已部分变质.
①请你对实验进行评价(假定实验操作过程准确无误):_________
A.该实验不能证明关于“部分变质”的推测
B.该实验可以证明关于“部分变质”的推测
C.若样品中混有少量氢氧化钾,也能使其质量百分数变小
②在用氢氧化钠固体配制溶液过程中,下列操作中也会造成氢氧化钠质量百分数偏小的是________(填字母)。
A.在称量时,把氢氧化钠样品放在称量纸上进行称量
B.在溶解过程中,有少量液体溅出
C.在转移过程中,烧杯和玻璃棒没有进行洗涤
D.在定容时,滴加蒸馏水超过刻度线,用滴管从容量瓶中小心取出多余液体至液体凹液面与刻度线水平
【答案】18.4 27.2 250mL容量瓶 0.143 71.25% BC ABCD
【解析】
(1)①根据c=![]() 计算;②根据溶液稀释前后物质的量不变即c(稀)V(稀)=c(浓)V(浓)计算所需浓硫酸的体积;根据配制步骤有计算、量取、稀释、移液、洗涤、定容、摇匀等操作选择仪器;
计算;②根据溶液稀释前后物质的量不变即c(稀)V(稀)=c(浓)V(浓)计算所需浓硫酸的体积;根据配制步骤有计算、量取、稀释、移液、洗涤、定容、摇匀等操作选择仪器;
(2)慢慢滴入硫酸溶液18.60ml时,测得溶液正好显中性,说明恰好生成Na2SO4,根据钠守恒和质量守恒列式计算解出NaOH、Na2CO3的物质的量,然后求出氢氧化钠的物质的量浓度以及质量百分数;①根据上述计算结果分析判断;②根据c=![]() 分析判断。
分析判断。
(1)①浓H2SO4的物质的量浓度c(H2SO4)=![]() =
=![]() =18.4mol/L,故答案为:18.4;
=18.4mol/L,故答案为:18.4;
②根据稀释定律,稀释前后溶质的物质的量不变,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=250mL×2.0mol/L,解得:x≈27.2,所以量取的浓硫酸体积是27.2mL;配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,一般用量筒量取(用到胶头滴管),在烧杯中稀释,冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为玻璃棒、烧杯、胶头滴管、量筒、250mL容量瓶,则缺少仪器250mL容量瓶,故答案为:27.2;250mL容量瓶;
(2)慢慢滴入0.1000mol/L的硫酸溶液18.60mL时,硫酸的物质的量为0.001860mol,测得溶液正好显中性,说明溶液中只有溶质Na2SO4,其物质的量为0.001860mol,设20.00mL待测液中NaOH、Na2CO3的物质的量分别为xmol、ymol,根据钠守恒有xmol+ymol×2=0.001860mol×2,根据质量守恒有40x+106y=2.000g×![]() ,解得:x=0.00286mol、y=0.00043mol,氢氧化钠的质量为0.00286mol×40g/mol=0.1144g,物质的量浓度
,解得:x=0.00286mol、y=0.00043mol,氢氧化钠的质量为0.00286mol×40g/mol=0.1144g,物质的量浓度![]() =0.143moL/mol,样品中NaOH的质量百分数为
=0.143moL/mol,样品中NaOH的质量百分数为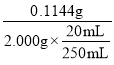 ×100%=71.25%,故答案为:0.143;71.25%;
×100%=71.25%,故答案为:0.143;71.25%;
①由上述计算结果可知,样品中混有少量碳酸钠,可以证明样品“部分变质”的推测;等质量的KOH和NaOH,KOH的物质的量小于NaOH,中和时,KOH需要硫酸的体积小于等质量的NaOH中和硫酸的体积,所以样品中混有少量氢氧化钾,会导致滴入的硫酸体积偏小,故C正确;故答案为:BC;
②A.在称量时,把氢氧化钠样品放在称量纸上进行称量,氢氧化钠具有吸湿性,易潮解,导致称出的氢氧化钠质量偏少,溶质的物质的量偏小,根据c=![]() 分析,氢氧化钠浓度减小,质量百分数偏小,故A正确;B.在溶解过程中,少量液体溅出,导致溶质的物质的量偏小,根据c=
分析,氢氧化钠浓度减小,质量百分数偏小,故A正确;B.在溶解过程中,少量液体溅出,导致溶质的物质的量偏小,根据c=![]() 分析,氢氧化钠浓度减小,质量百分数偏小,故B正确;C.在转移过程中,烧杯和玻璃棒没有进行洗涤,溶质的物质的量偏小,根据c=
分析,氢氧化钠浓度减小,质量百分数偏小,故B正确;C.在转移过程中,烧杯和玻璃棒没有进行洗涤,溶质的物质的量偏小,根据c=![]() 分析,氢氧化钠浓度减小,质量百分数偏小,故C正确;D.在定容时,滴加蒸馏水超过刻度线,用滴管从容量瓶中小心取出多余液体至液体凹液面与刻度线水平,溶质的物质的量偏小,根据c=
分析,氢氧化钠浓度减小,质量百分数偏小,故C正确;D.在定容时,滴加蒸馏水超过刻度线,用滴管从容量瓶中小心取出多余液体至液体凹液面与刻度线水平,溶质的物质的量偏小,根据c=![]() 分析,氢氧化钠浓度减小,质量百分数偏小,故D正确;故答案为:ABCD。
分析,氢氧化钠浓度减小,质量百分数偏小,故D正确;故答案为:ABCD。

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案【题目】某温度下,在甲、乙、丙、丁四个恒容密闭容器中投入H2和I2,发生反应:H2(g)+I2(g) ![]() 2HI(g)。反应体系中各物质浓度的有关数据如下。
2HI(g)。反应体系中各物质浓度的有关数据如下。
容器 | 起始浓度 | 平衡浓度 | |
c(H2)/(mol·L-1) | c(I2)/(mol·L-1) | c(HI)/(mol·L-1) | |
甲 | 0.01 | 0.01 | 0.004 |
乙 | 0.01 | 0.02 | a |
丙 | 0.02 | 0.01 | b |
丁 | 0.02 | 0.02 | c |
下列判断不正确的是
A. HI的平衡浓度:a=b>0.004,c=0.008 B. 平衡时,H2的转化率:丁>甲
C. 平衡时,乙中H2的转化率大于20% D. 丙中条件下,该反应的平衡常数K=0.25
【题目】CO、H2、CH3OH均是清洁能源。
(1)已知部分化学键键能数据如下:
化学键 | C | O=O | C=O | C-O |
E/(kJ mol-1) | 958.5 | 497 | 745 | 351 |
2CO(g) +O2(g)==2CO2(g) ![]() H1 H2O(g)+CO(g)==H2(g) + CO2(g)
H1 H2O(g)+CO(g)==H2(g) + CO2(g) ![]() H2 = -41 kJmol-1
H2 = -41 kJmol-1
CH3OH(g)+ 3/2O2(g)==CO2(g)+2H2O(g) ![]() H3 = -660kJmol-1
H3 = -660kJmol-1
则△H1=_____ kJmol-1,反应CO(g)+2H2(g)![]() CH3OH(g)的△H=_____ kJmol-1。
CH3OH(g)的△H=_____ kJmol-1。
(2)一定条件下,在容积为2 L的密闭容器Q中充入a mol CO与b molH2合成甲醇:CO(g) +2H2(g) ![]() CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。
CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。

①压强相同时,温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者之间的相对大小为t1___ t2(填“>”、“<”、“=”或“无法确定”)。
②P1_____P2(填“>”、“<”、“=”或“无法确定”)。
③若a =2,b=4,则压强为P1、温度为T1时该反应的平衡常数K=______________。
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体,则反应开始时,v(CH3OH)正_____v(CH3OH)逆(填“>”、“<”、“=”或“无法确定”)。