题目内容
a mo1 FeS与b mol FeO投入到稀硝酸溶液中充分反应后无固体剩余,得到Fe(NO3)3相H2SO4的混合溶液,并产生NO气体。则反应中氧化产物与还原产物的物质的量之比为
A.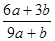 | B.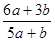 | C.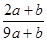 | D.不能确定 |
A
试题分析:该反应中元素的化合价变化为:S元素化合价由-2价变为+6价,失去8个电子。Fe元素化合价由+2价变为+3价,失去1个电子。N元素化合价由+5价变为+2价,得到3个电子。所以反应中氧化产物是Fe(NO3)3和H2SO4,还原产物是NO。设生成NO的物质的量为x,根据电子得失守恒可知,a×[6-(-2)+(3-2)]mol+b×(3-2)mol=(5-2)×x,解得x=
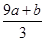 mol。根据原子守恒知,氧化产物的物质的量=(a+b)mol+amol=(2a+b)mol,所以氧化产物和还原产物的物质的量之比=
mol。根据原子守恒知,氧化产物的物质的量=(a+b)mol+amol=(2a+b)mol,所以氧化产物和还原产物的物质的量之比=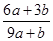 ,答案选A。
,答案选A。
练习册系列答案
相关题目
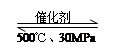 2NH3(g)△H=-38.6kJ·mol-1
2NH3(g)△H=-38.6kJ·mol-1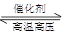 2NH3(g)△H﹤0,升高温度,可使反应速率增大,反应逆向移动
2NH3(g)△H﹤0,升高温度,可使反应速率增大,反应逆向移动