��Ŀ����
����Ŀ��N2��H2�ϳ�NH3�������仯��ͼ��ʾ���÷�Ӧ���Ȼ�ѧ����ʽ�ǣ� ��
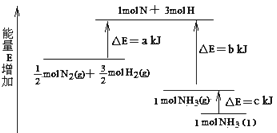
A.N2(g)��3H2(g)��2NH3(l) ��H��2(a-b-c)kJ/mol
B.N2(g)��3H2(g)��2NH3(g) ��H��2(b-a)kJ/mol
C.1/2 N2(g)��3/2H2(g)��NH3(l) ��H��(b��c-a)kJ/mol
D.1/2 N2(g)��3/2H2(g)��NH3(g) ��H��(a��b)kJ/mol
���𰸡�A
��������
����ͼ��![]() molN2(g)+
molN2(g)+![]() molH2(g)��������1molNH3(g)��������(b-a)kJ�����
molH2(g)��������1molNH3(g)��������(b-a)kJ�����![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) ��H=(a-b)kJ/mol����1mol��NH3(g)ת��Ϊ1mol��NH3(l)�ų�������ΪckJ�������У�
H2(g)=NH3(g) ��H=(a-b)kJ/mol����1mol��NH3(g)ת��Ϊ1mol��NH3(l)�ų�������ΪckJ�������У�![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ��H=(a-b-c)kJ/mol������N2(g)+3H2(g)=2NH3(1) ��H=2(a-b-c)kJmol-1����ѡA��
H2(g)=NH3(l) ��H=(a-b-c)kJ/mol������N2(g)+3H2(g)=2NH3(1) ��H=2(a-b-c)kJmol-1����ѡA��

 �¿α�������������ҵ�������γ�����ϵ�д�
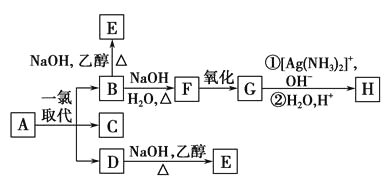
�¿α�������������ҵ�������γ�����ϵ�д�����Ŀ�����������LiFePO4��һ��������������ӵ�صĵ缫���ϡ�ij�����������졢﮻�ʯLiAl��SiO3��2��������Ca2+��Mg2+���Σ���̼�۵�ԭ����������������ﮡ�����Ҫ����������ͼ��

��֪��2LiAl��SiO3��2+H2SO4(Ũ)![]() Li2SO4+Al2O3��4SiO2��H2O��
Li2SO4+Al2O3��4SiO2��H2O��
�¶�/�� | 20 | 40 | 60 | 80 | |
�ܽ��(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 | |
�ܽ��(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
��1�����������пɷ����Al2O3����ͼ��ʾ����д�����ɳ��������ӷ���ʽ___��
![]()
��2�����������Ҫ�ɷ��ǣ�___���ѧʽ����
��3������Һ���м��뱥��Na2CO3��Һ�����˺�������ˮϴ������ԭ����___��
��4��д���ڸ�����������������﮵Ļ�ѧ����ʽ��___��
��5����������﮵���ܷ�ӦΪ��FePO4+Li![]() LiFePO4������еĹ������ʿɴ���Li+����д���õ�طŵ�ʱ��������Ӧ��___�����øõ�ص�ⱥ��ʳ��ˮ�����ص缫��Ϊ���Ե缫������������������4480mL���壨��״��������ʱ���õ������﮵�����Ϊ___��
LiFePO4������еĹ������ʿɴ���Li+����д���õ�طŵ�ʱ��������Ӧ��___�����øõ�ص�ⱥ��ʳ��ˮ�����ص缫��Ϊ���Ե缫������������������4480mL���壨��״��������ʱ���õ������﮵�����Ϊ___��
����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��CO2(g)+H2(g)CO(g)+H2O(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ�����
t/�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
(1)�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=___����֪��K1000����K800������÷�Ӧ��__��Ӧ��(��������������������)��
(2)��֪��800��ʱ���÷�Ӧ��ƽ�ⳣ��K1=0.9������¶��·�ӦCO(g)��H2O(g)![]() CO2(g)��H2(g)��ƽ�ⳣ��K2=___��
CO2(g)��H2(g)��ƽ�ⳣ��K2=___��
(3)���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������__��
A��������ѹǿ����
B�����������c(CO)����
C��v��(H2)=v��(H2O)
D��c(CO2)=c(CO)
(4)ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)c(H2)=c(CO)c(H2O)�����жϴ�ʱ���¶�Ϊ__�档