题目内容
【题目】As2O3在医药、电子等领域有重要应用。某含砷元素(As)的工业废水经如图1流程转化为粗产品。
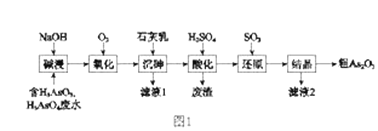
(1)“碱浸”的目的是将废水中的H3AsO3和H3AsO4转化为盐。H3AsO4转化为Na3AsO4反应的化学方程式是_______________________________。
(2)“氧化”时,1molAsO33-转化为AsO43-至少需要O2______ mol。
(3)“沉砷”是将砷元素转化为Ca5(AsO4)3OH沉淀,发生的主要反应有:
a.Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq) △H<0
Ca2+(aq)+2OH-(aq) △H<0
b.5Ca2++OH-+3AsO43-![]() Ca5(AsO4)3OH △H>0
Ca5(AsO4)3OH △H>0
研究表明:“沉砷”的最佳温度是85℃。 用化学平衡原理解释温度高于85℃后,随温度升高沉淀率下降的原因是_____________________。
(4)“还原”过程中H3AsO4转化为H3AsO3,反应的化学方程式是_______________________。
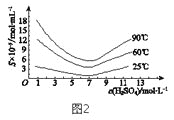
(5)“还原”后加热溶液,H3AsO3分解为As2O3,同时结晶得到粗As2O3。As2O3在不同温度和不同浓度硫酸中的溶解度(S)曲线如图2所示。为了提高粗As2O3的沉淀率,“结晶”过程进行的操作是_______。
(6)下列说法中,正确的是 ______ (填字母)。
a.粗As2O3中含有CaSO4
b.工业生产中,滤液2可循环使用,提高砷的回收率
c.通过先“沉砷”后“酸化”的顺序,可以达到富集砷元素的目的
【答案】 H3AsO4+3NaOH═Na3AsO4+3H2O 0.5 温度升高,反应a平衡逆向移动,c(Ca2+)下降,反应b平衡逆向移动,Ca5(AsO4)3OH沉淀率下降 H3AsO4+H2O+SO2═H3AsO3+H2SO4 调硫酸浓度约为7molL-1,冷却至25℃,过滤 abc
【解析】试题分析:(1)H3AsO4与氢氧化钠发生中和反应生成Na3AsO4;(2)根据电子守恒计算1molAsO33-转化为AsO43-至少需要O2的物质的量;(3)温度升高,Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq) △H<0,平衡逆向移动,c(Ca2+)、c(OH-)下降,所以反应b平衡逆向移动;(4)H3AsO4被SO2还原成H3AsO3;(5)根据图2,As2O3的溶解度在25℃、硫酸的浓度在7molL-1时最小;(6)CaSO4微溶于水;滤液2含有少量As2O3、硫酸;“沉砷”生成Ca5(AsO4)3OH可以富集砷元素;
Ca2+(aq)+2OH-(aq) △H<0,平衡逆向移动,c(Ca2+)、c(OH-)下降,所以反应b平衡逆向移动;(4)H3AsO4被SO2还原成H3AsO3;(5)根据图2,As2O3的溶解度在25℃、硫酸的浓度在7molL-1时最小;(6)CaSO4微溶于水;滤液2含有少量As2O3、硫酸;“沉砷”生成Ca5(AsO4)3OH可以富集砷元素;
解析:(1)H3AsO4与氢氧化钠发生中和反应生成Na3AsO4,反应方程式是H3AsO4+3NaOH═Na3AsO4+3H2O;(2)1molAsO33-转化为AsO43-失电子2mol,1mol氧气得电子4mol,根据电子守恒,需要O2的物质的量![]() ;(3)温度升高,Ca(OH)2(s)
;(3)温度升高,Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq) △H<0,平衡逆向移动,c(Ca2+)、c(OH-)下降,反应b平衡逆向移动,所以随温度升高沉淀率下降;(4)H3AsO4被SO2还原成H3AsO3反应的化学方程式是H3AsO4+H2O+SO2═H3AsO3+H2SO4;(5)根据图2,As2O3的溶解度在25℃、硫酸的浓度在7molL-1时最小,为了提高粗As2O3的沉淀率,“结晶”过程进行的操作是调硫酸浓度约为7molL-1,冷却至25℃,过滤;(6)CaSO4微溶于水,钙离子未完全除去,所以粗As2O3中含有CaSO4,故a正确;滤液2含有少量As2O3、硫酸,滤液2可循环使用,提高砷的回收率,故b正确;“沉砷”生成Ca5(AsO4)3OH可以富集砷元素,故c正确。
Ca2+(aq)+2OH-(aq) △H<0,平衡逆向移动,c(Ca2+)、c(OH-)下降,反应b平衡逆向移动,所以随温度升高沉淀率下降;(4)H3AsO4被SO2还原成H3AsO3反应的化学方程式是H3AsO4+H2O+SO2═H3AsO3+H2SO4;(5)根据图2,As2O3的溶解度在25℃、硫酸的浓度在7molL-1时最小,为了提高粗As2O3的沉淀率,“结晶”过程进行的操作是调硫酸浓度约为7molL-1,冷却至25℃,过滤;(6)CaSO4微溶于水,钙离子未完全除去,所以粗As2O3中含有CaSO4,故a正确;滤液2含有少量As2O3、硫酸,滤液2可循环使用,提高砷的回收率,故b正确;“沉砷”生成Ca5(AsO4)3OH可以富集砷元素,故c正确。