题目内容
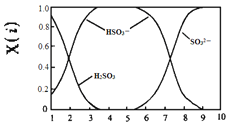
【题目】为验证氯元素比硫元素非金属性强,某化学实验小组设计如下实验,请回答下列问题:

(1)A中药品足量,发生的化学反应方程式____,当生成2.24 L Cl2(标况)时,被氧化的浓盐酸的物质的量为____;
(2)B中试剂为_______,该装置的作用是_______;
(3)C中盛有硫化钾溶液,该装置的现象是______;
(4)在D的KI溶液中添加少量_____,通过观察到________的现象,可以证明氯元素的非金属性大于碘元素。指出整个实验设计的不足之处_____;
(5)请阅读下列信息:
①硫化氢的水溶液酸性比氯化氢的弱 ②S2Cl2分子中氯元素显-1价 ③铜和氯气在加热条件下反应生成氯化铜,铜和硫在加热条件下反应生成硫化亚铜 ④沸点:硫磺>氯气 ⑤高氯酸的酸性大于硫酸
能证明氯元素的非金属性比硫元素强的是______(填序号)
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 0.2mol 饱和氯化钠溶液 除去Cl2中HCl 产生淡黄色沉淀 淀粉 溶液变蓝 没有尾气吸收Cl2装置 ②③⑤
MnCl2+Cl2↑+2H2O 0.2mol 饱和氯化钠溶液 除去Cl2中HCl 产生淡黄色沉淀 淀粉 溶液变蓝 没有尾气吸收Cl2装置 ②③⑤
【解析】
(1)A装置用于制取氯气,加热条件下浓盐酸和二氧化锰反应生成氯化锰、氯气和水,所以分液漏斗中盛放的是浓盐酸、烧瓶中加入的是MnO2,化学方程式为 MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,根据化学方程式可知,生成1molCl2,有2molHCl被氧化,则生成
MnCl2+Cl2↑+2H2O,根据化学方程式可知,生成1molCl2,有2molHCl被氧化,则生成![]() =0.1molCl2,被氧化的HCl为0.2mol;答案为MnO2+4HCl(浓)
=0.1molCl2,被氧化的HCl为0.2mol;答案为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,0.2mol。
MnCl2+Cl2↑+2H2O,0.2mol。
(2)浓盐酸具有挥发性,所以生成的氯气中含有HCl,饱和食盐水能溶解HCl且能抑制氯气的溶解,可以用饱和食盐水除去氯气中的HCl,所以广口瓶中盛放的是饱和食盐水,其作用是除去氯气中的HCl;答案为饱和食盐水;除去氯气中的HCl。
(3)要证明氯元素的非金属性比S元素强,可以用氯气氧化硫离子生成S来实现,离子方程式为Cl2+S2-=S↓+2Cl-,现象是生成淡黄色沉淀S;答案为有淡黄色沉淀生成。
(4)根据I2遇淀粉变蓝色,检验I2单质的生成,因而在D的KI溶液中添加少量淀粉,发生Cl2+2KI=2KCl+I2,I2遇淀粉变蓝色,可以证明Cl2置换出了I2,证明氯元素的非金属性大于碘元素,因为Cl2是有毒气体,不能任意排放到空气中,所以实验装置最后接一个盛放烧碱溶液装置,目的是吸收反应后剩余的气体,防止污染空气;
答案为淀粉,变蓝色。没有尾气吸收Cl2的装置。
(5)①气态氢化物溶液的酸性强弱与非金属性强弱判断无关,应该比较其稳定性,故①错误;
②S2Cl2分子中氯元素显-1价,则硫元素显+1价,说明形成的共用电子对偏向氯元素,偏离硫元素,说明吸引电子对Cl>S,可以说明硫元素的非金属性比氯元素的非金属性弱,故②正确。
③氯气将铜元素氧化成最高价态,呈现+2价,而硫只能氧化铜元素生成+1价,说明氯气的氧化性更强,说明硫元素的非金属性比氯元素的非金属性弱,故③正确;
④因为硫磺和氯气均为分子晶体,沸点:硫磺>氯气, 只说明硫磺分子间作用力大于氯气分子间作用力,与非金属性强弱判断无关,故④错误;
⑤最高价氧化物对应水化物的酸性强说明非金属性强,高氯酸的酸性大于硫酸,说明硫元素的非金属性比氯元素的非金属性弱,故⑤正确;答案为②③⑤。

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案【题目】下列方法中,不能用于实验室制取氨的是
A. 加热试管中的氯化铵固体
B. 在烧瓶中将熟石灰和氯化铵混合,加水调成泥状后加热
C. 将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
D. 将烧瓶中的浓氨水加热
【题目】苯胺为无色液体,还原性强,易被氧化;有碱性,与酸反应生成盐。常用硝基苯与H2制备:
![]() +3H2
+3H2![]()
![]() +2H2O。
+2H2O。
其部分装置及有关数据如下:
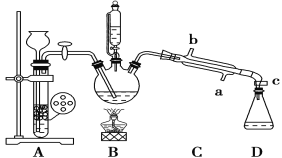
项目 | 沸点/℃ | 密度(g/mL) | 溶解性 |
硝基苯 | 210.9 | 1.20 | 不溶于水,易溶于乙醇、乙醚 |
苯胺 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚 |
乙醚 | 34.6 | 0.71 | 不溶于水,易溶于硝基苯、苯胺 |
实验步骤:
①检查装置的气密性,连接好C处冷凝装置的冷水。
②先向三颈烧瓶中加入沸石及硝基苯,再取下恒压分液漏斗,换上温度计。
③打开装置A、B间活塞,通入H2一段时间。
④点燃B处的酒精灯,加热,使温度维持在140℃进行反应。
⑤反应结束后,关闭装置A、B间活塞,加入生石灰。
⑥调整好温度计的位置,继续加热,收集182~186 ℃馏分,得到较纯苯胺。
回答下列问题:
(1)步骤⑥中温度计水银球的位置在________。
(2)下列关于实验的叙述中,错误的是________。
A.冷凝管的冷水应该从b进从a出
B.实验开始时,温度计水银球应插入反应液中,便于控制反应液的温度
C.装置A中应使用锌粉,有利于加快生成H2的速率
D.加入沸石的目的是防止暴沸
(3)若实验中步骤③和④的顺序颠倒,则实验中可能产生的后果是_______。
(4)蒸馏前,步骤⑤中加入生石灰的作用是_______。
(5)有学生质疑反应完成后,直接蒸馏得到苯胺的纯度不高,提出以下流程:
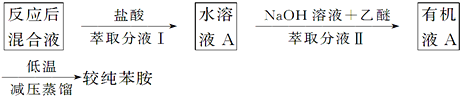
苯胺在酸性条件下生成盐酸苯胺被水萃取,在碱性溶液中又被放有机溶剂反萃取,这种萃取——反萃取法简称反萃。实验中反萃的作用是___;在分液漏斗中进行萃取分液时,应注意不时放气,其目的是____。