题目内容
【题目】(12)烷烃A只可能有三种一氯取代产物B、C和D。C的结构简式是 。B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。以上反应及B的进一步反应如下所示。
。B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。以上反应及B的进一步反应如下所示。

请回答下列问题:
(1)A的结构简式是_______________H的结构简式是________________
(2)B转化为F属于________反应,B转化为E的反应属于________反应(填反应类型名称)。
(3)写出F转化为G的化学方程式_____________ 。
(4)1.16 g H与足量NaHCO3作用,标准状况下可得CO2的体积是______mL。
(5)写出反应①的方程式______________
【答案】除标注外,其它每空2分,共12分
(1) (CH3)3CCH2CH3; (CH3)3CCH2COOH
(2)取代(水解) ;消去 (每空1分)
(3) 2(CH3)3CCH2CH2OH+O2![]() 2(CH3)3CCH2CHO+2H2O
2(CH3)3CCH2CHO+2H2O
(4)224
(5)(CH3)3CCH2CHO+2Ag(NH3)2OH→(CH3)3CCH2COONH4+2Ag↓+3NH3+H2O
【解析】
烷烃A只可能有三种一氯取代产物B、C和D,C的结构简式是: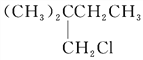 ,故A为(CH3)3CCH2CH3,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E,故E为(CH3)3CCH=CH2,B在氢氧化钠水溶液下生成F,F为醇,F氧化生成G,G能与银氨溶液反应,G含有醛基—CHO,故B为(CH3)3CCH2CH2Cl,F为(CH3)3CCH2CH2OH,G为(CH3)3CCH2CHO,H为(CH3)3CCH2COOH,D为(CH3)3CCH2ClCH3。1)A的结构简式是(CH3)3CCH2CH3,H的结构简式是(CH3)3CCH2COOH;(2)B转化为F属于取代反应或水解反应,B转化为E的反应属于消去反应;(3)F转化为G的化学方程式:2(CH3)3CCH2CH2OH+O2
,故A为(CH3)3CCH2CH3,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E,故E为(CH3)3CCH=CH2,B在氢氧化钠水溶液下生成F,F为醇,F氧化生成G,G能与银氨溶液反应,G含有醛基—CHO,故B为(CH3)3CCH2CH2Cl,F为(CH3)3CCH2CH2OH,G为(CH3)3CCH2CHO,H为(CH3)3CCH2COOH,D为(CH3)3CCH2ClCH3。1)A的结构简式是(CH3)3CCH2CH3,H的结构简式是(CH3)3CCH2COOH;(2)B转化为F属于取代反应或水解反应,B转化为E的反应属于消去反应;(3)F转化为G的化学方程式:2(CH3)3CCH2CH2OH+O2![]() 2(CH3)3CCH2CHO+2H2O ;(4)1.16 g(CH3)3CCH2COOH的物质的量为
2(CH3)3CCH2CHO+2H2O ;(4)1.16 g(CH3)3CCH2COOH的物质的量为![]() =0.01 mol,由(CH3)3CCH2COOH+NaHCO3―→(CH3)3CCH2COONa+H2O+CO2↑可知,生成CO2的物质的量为0.01 mol,二氧化碳的体积是0.01 mol×22.4 L·mol-1=0.224 L=224 mL;(5)反应①的化学方程式为:(CH3)3CCH2CHO+2[Ag(NH3)2]OH
=0.01 mol,由(CH3)3CCH2COOH+NaHCO3―→(CH3)3CCH2COONa+H2O+CO2↑可知,生成CO2的物质的量为0.01 mol,二氧化碳的体积是0.01 mol×22.4 L·mol-1=0.224 L=224 mL;(5)反应①的化学方程式为:(CH3)3CCH2CHO+2[Ag(NH3)2]OH![]() (CH3)3CCH2COONH4+2Ag↓+3NH3+H2O。
(CH3)3CCH2COONH4+2Ag↓+3NH3+H2O。

 名校课堂系列答案
名校课堂系列答案【题目】苯胺为无色液体,还原性强,易被氧化;有碱性,与酸反应生成盐。常用硝基苯与H2制备:
![]() +3H2
+3H2![]()
![]() +2H2O。
+2H2O。
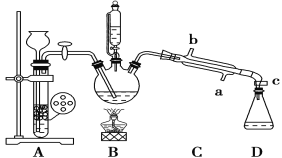
其部分装置及有关数据如下:
项目 | 沸点/℃ | 密度(g/mL) | 溶解性 |
硝基苯 | 210.9 | 1.20 | 不溶于水,易溶于乙醇、乙醚 |
苯胺 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚 |
乙醚 | 34.6 | 0.71 | 不溶于水,易溶于硝基苯、苯胺 |
实验步骤:
①检查装置的气密性,连接好C处冷凝装置的冷水。
②先向三颈烧瓶中加入沸石及硝基苯,再取下恒压分液漏斗,换上温度计。
③打开装置A、B间活塞,通入H2一段时间。
④点燃B处的酒精灯,加热,使温度维持在140℃进行反应。
⑤反应结束后,关闭装置A、B间活塞,加入生石灰。
⑥调整好温度计的位置,继续加热,收集182~186 ℃馏分,得到较纯苯胺。
回答下列问题:
(1)步骤⑥中温度计水银球的位置在________。
(2)下列关于实验的叙述中,错误的是________。
A.冷凝管的冷水应该从b进从a出
B.实验开始时,温度计水银球应插入反应液中,便于控制反应液的温度
C.装置A中应使用锌粉,有利于加快生成H2的速率
D.加入沸石的目的是防止暴沸
(3)若实验中步骤③和④的顺序颠倒,则实验中可能产生的后果是_______。
(4)蒸馏前,步骤⑤中加入生石灰的作用是_______。
(5)有学生质疑反应完成后,直接蒸馏得到苯胺的纯度不高,提出以下流程:
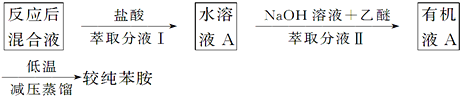
苯胺在酸性条件下生成盐酸苯胺被水萃取,在碱性溶液中又被放有机溶剂反萃取,这种萃取——反萃取法简称反萃。实验中反萃的作用是___;在分液漏斗中进行萃取分液时,应注意不时放气,其目的是____。