��Ŀ����
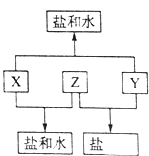
����Ŀ��ij�����A������KAl��SO4��2��Al2O3��Fe2O3 �� ��һ�������¿�ʵ����ͼ��ʾ������֮��ı仯��
�ݴ˻ش��������⣺
��1�����IJ��ж�����Һ�ͳ����ķ����ȡ�ķ����� ��
��2������������ͼ��Ӧ��ϵ��д������B��D��E�������ʵĻ�ѧʽ
����B������D����ҺE�� _��
��3��д���١��ڡ���������Ӧ�����ӷ���ʽ���������ӷ�Ӧ��д���仯ѧ����ʽ��
���������� ��
���𰸡�
��1������
��2��Al2O3��Fe2O3��K2SO4����NH4��2SO4��NH3��H2O
��3��Al2O3+2OH��=2AlO2��+H2O��Al3++3NH3 �� H2O=Al��OH��3��+3NH4+��2Al��OH��3 ![]() Al2O3+3H2O
Al2O3+3H2O
���������⣺�����̿�֪��Al2O3��Fe2O3������ˮ�������CΪAl2O3��Fe2O3 �� ����������Ӧ�������DΪFe2O3 �� ��Ӧ�ڢ������ɵij���ΪAl��OH��3 �� ���ȷֽ�����BΪAl2O3 �� ��Ӧ��ΪKAl��SO4��2����ˮ�ķ�Ӧ������ҺEΪK2SO4����NH4��2SO4��NH3��H2O����1�������IJ��ж�����Һ�ͳ����ķ��뷽��Ϊ���ˣ����Դ��ǣ����ˣ���2��������������֪��BΪAl2O3 �� DΪFe2O3 �� EΪK2SO4����NH4��2SO4��NH3��H2O�����Դ��ǣ�Al2O3��Fe2O3��K2SO4����NH4��2SO4��NH3 �� H2O����3����Ӧ��ΪAl2O3+2OH��=2AlO2��+H2O����Ӧ��ΪAl3++3NH3 �� H2O=Al��OH��3��+3NH4+ �� ��Ӧ��Ϊ2Al��OH��3 ![]() Al2O3+3H2O�����Դ��ǣ�Al2O3+2OH��=2AlO2��+H2O��Al3++3NH3��H2O=Al��OH��3��+3NH4+��2Al��OH��3
Al2O3+3H2O�����Դ��ǣ�Al2O3+2OH��=2AlO2��+H2O��Al3++3NH3��H2O=Al��OH��3��+3NH4+��2Al��OH��3 ![]() Al2O3+3H2O��
Al2O3+3H2O��