题目内容
15.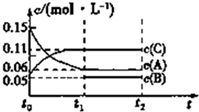 向某密闭容器中加入0.3mol A、0.1mol C和一定量的B三种气体.一定条件下发生反应,各物质的浓度随时间变化如甲图所示[t0~t1阶段的c(B)变化未画出],t1时刻达到平衡,反应过程中混合气体的平均相对分子质量始终不变.下列说法正确的是( )
向某密闭容器中加入0.3mol A、0.1mol C和一定量的B三种气体.一定条件下发生反应,各物质的浓度随时间变化如甲图所示[t0~t1阶段的c(B)变化未画出],t1时刻达到平衡,反应过程中混合气体的平均相对分子质量始终不变.下列说法正确的是( )| A. | 该容器的体积为2L | |
| B. | 起始时B的物质的量为0.08mol | |
| C. | 该反应的方程式为3A=2C+B | |
| D. | 若t1=15 s,则用B的浓度变化表示的t0~t1阶段的平均反应速率为0.002 mol/(L•s) |
分析 A、反应中A的浓度变化为0.15mol/L-0.06mol/L=0.09mol/L,C的浓度变化为0.11mol/L-0.05mol/L=0.06mol/L,根据浓度等于物质的量和体积的比值来计算;
B、根据A、C浓度变化量确定二者的系数之比以及反应过程中混合气体的平均相对分子质量始终不变,得到反应是前后气体的系数和相等的反应,在据此得到起始时B的物质的量浓度进而计算初始物质的量;
C、根据A、C浓度变化量确定二者的系数之比以及反应过程中混合气体的平均相对分子质量始终不变,得到反应是前后气体的系数和相等的反应,确定B的位置和系数,书写方程式;
D、若t1=15 s,则用B的浓度变化表示的t0~t1阶段的平均反应速率=$\frac{△c}{△t}$来进行计算.
解答 解:A、反应中A的初始浓度0.15mol/L,C的初始浓度为0.05mol/L,浓度等于物质的量和体积的比值,所以$\frac{0.3mol}{V}$=0.15mol/L、$\frac{0.1mol}{V}$=0.05mol/L,解得V=2L,故A正确;
B、反应中A的浓度变化为0.15mol/L-0.06mol/L=0.09mol/L,C的浓度变化为0.11mol/L-0.05mol/L=0.06mol/L,所以A、C的系数之比是3:2,反应过程中混合气体的平均相对分子质量始终不变,得到反应是前后气体的系数和相等的反应,所以B的物质的量浓度变化量是0.03mol/L,起始浓度是0.02mol/L,物质的量是0.04mol,故B错误;
C、A、B、C在方程式的系数之比是3:1:2,A是反应物,B、C是产物,反应最终达到了平衡,属于可逆反应,即反应方程式为:3A?2C+B,故C错误;
D、若t1=15 s,则用B的浓度变化表示的t0~t1阶段的平均反应速率=$\frac{△c}{△t}$=$\frac{0.03mol/L}{15s}$=0.002mol/(L•s),故D正确;
故选AD.
点评 本题考查学生化学反应中化学反应速率的有关计算等知识,注意结论的使用以及方程式系数的确定是关键,难度中等.

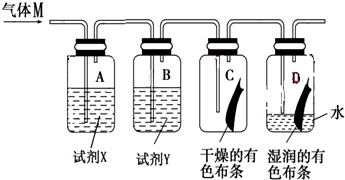
(1)装置A、B中的试剂X和试剂Y分别是b(填字母代号).
a.NaOH溶液 浓硫酸 b.NaCl溶液 浓硫酸 c.浓硫酸 石灰水
(2)若C中有色布条不褪色,D中有色布条褪色.则具有漂白性的物质是次氯酸(填物质名称),该实验证明氯气能与水反应,反应的离子方程式为Cl+H2O=H++Cl-+HClO.
(3)从绿色化学的角度分析,上述实验装置图中存在一处缺陷,改正的方法是加一个尾气处理装置,该尾气处理装置内发生反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
(4)实验完毕后,将D中的水溶液(呈黄绿色)取出,分别加入两支试管中,进行如下实验
| 实验编号 | 滴加的试剂 | 实验现象 | 证明存在的微粒 (填微粒符号) |
| A | AgNO3 溶液 | a.产生白色沉淀 | b.Cl- |
| B | 紫色石蕊溶液 | c.先变红色后褪色 | d.H+,HClO |
| A. | 硅是非金属 | |
| B. | 它是非金属氧化物 | |
| C. | 二氧化硅能跟氢氧化钠反应生成盐和水 | |
| D. | 它的对应水化物是弱酸,能溶于水 |



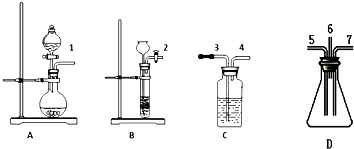
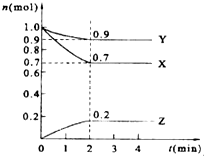 某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.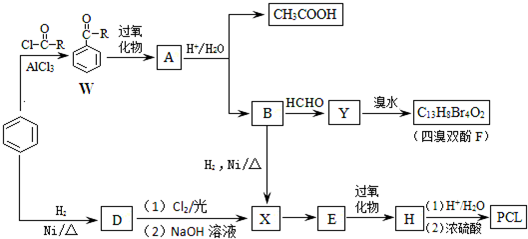
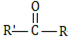 $\stackrel{过氧化物}{→}$
$\stackrel{过氧化物}{→}$ 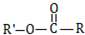 (R,R′代表烃基)
(R,R′代表烃基)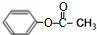 .
.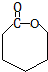 .
.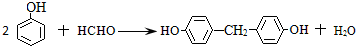 .
. .
.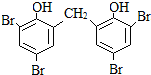 或
或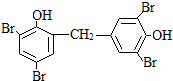 .
.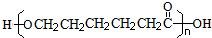 .
.