题目内容
19.关于乙烯基乙炔(CH≡C-CH═CH2)分子的说法错误的是( )| A. | 能使酸性KMnO4溶液褪色 | |
| B. | 乙烯基乙炔能与Br2发生加成反应 | |
| C. | 乙烯基乙炔分子内含有两种官能团 | |
| D. | 等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同 |
分析 乙烯基乙炔(CH≡C-CH═CH2)中含碳碳三键、碳碳双键,结合炔烃、烯烃的性质来解答.
解答 解:A.含碳碳三键、碳碳双键,均能使酸性KMnO4溶液褪色,故A正确;
B.含碳碳三键、碳碳双键,均能与Br2发生加成反应,故B正确;
C.碳碳三键、碳碳双键均为官能团,共2种,故C正确;
D.二者最简式均为CH,含C、H的质量分数相同,则等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、炔烃性质的考查,选项D为解答的难点,题目难度不大.

练习册系列答案
相关题目
9.下列离子方程式正确的是( )
| A. | 氨水与亚硫酸溶液混合:NH3•H2O+H+═NH4++H2O | |
| B. | 将少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=2HClO+CaSO3↓ | |
| C. | 足量铁屑溶于稀硫酸:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 将Cl2通入FeSO4溶液中:Cl2+2Fe2+═2Fe3++2 Cl- |
7.下表是五种短周期元素的原子半径,最高正价及负化合价,下列叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/mm | 0.160 | 0.089 | 0.143 | 0.102 | 0.074 |
| 化合价 | +2 | +2 | +3 | +6,-2 | -2 |
| A. | L、M的单质与稀盐酸反应速率L<M | |
| B. | Q、T两元素间可形成两性化合物 | |
| C. | R、T两元素的氢化物分子间能形成氢键 | |
| D. | L、R两元素的简单离子的核外电子数可能相等 |
14.下列说法正确的是( )??
| A. | 苯不能使酸性KMnO4溶液褪色,与甲烷性质相似,因此苯为饱和烃 | |
| B. | 苯的结构简式为 ,有三个双键,可与溴水发生加成反应 ,有三个双键,可与溴水发生加成反应 | |
| C. | 苯的6个碳原子和6个氢原子在同一平面内 | |
| D. | 将1mL苯和1mL水充分混合后静置,二者互溶 |
4.向一密闭容器中充入1mol N2和3mol H2,在一定条件下发生反应(N2+3H2?2NH3).下列有关说法不正确的是( )
| A. | 达到化学平衡时,N2、H2和NH3的物质的量之比为1:3:2 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 | |
| C. | 达到化学平衡时,N2不能完全转化为NH3 | |
| D. | 达到化学平衡时,容器中气体的总压强不再发生变化 |
8.一定条件下反应2AB(g)?A2(g)+B2(g)达到平衡状态的标志是( )
| A. | 单位时间内生成nmolA2,同时消耗2n molAB | |
| B. | 容器中各组分的体积分数不随时间变化容器内 | |
| C. | AB的消耗速率等于A2的消耗速率 | |
| D. | 3种气体AB、A2、B2共存 |
3.下列所有元素组合,既可以形成离子化合物,又可形成共价化合物的一组是( )
| A. | H、C、O、K | B. | H、N、O | C. | H、O、S | D. | H、O、S、Na |

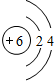 .
. ;写出C2B2的电子式
;写出C2B2的电子式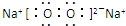 .
.