题目内容
11.A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲;D的L层电子数等于K、M两个电子层上的电子数之和.(1)写出A的原子结构示意图
 .
.(2)D的质子数和中子数相等,D的原子组成符号为3216S.
(3)用电子式表示A、D两元素形成AD2的过程:
 ;写出C2B2的电子式
;写出C2B2的电子式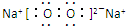 .
.(4)氢元素与B、D 均可以形成原子个数比为2:1的化合物,H2B的熔沸点高于H2D的原因是H2O分子之间存在氢键.
(5)写出甲和A的最高价氧化物反应的化学方式:2Na2O2+CO2=2Na2CO3+O2.
分析 A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲,固体甲为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,则D为S元素,据此解答.
解答 解:A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲,固体甲为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,则D为S元素.
(1)由上述分析可知,A为C元素,原子结构示意图为: ,故答案为:
,故答案为: ;
;
(2)D为S元素,原子的质子数和中子数相等,质量数为32,D的原子组成符号为3216S,故答案为:3216S;
(3)A、D两元素形成CO2,用电子式表示其形成过程为: ,
,
C2B2为Na2O2,电子式是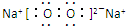 ,
,
故答案为: ;
;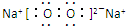 ;
;
(4)氢元素与O、S均可以形成原子个数比为2:1的化合物分别为H2O、H2S,由于H2O分子之间存在氢键,故H2O的沸点高于H2S,
故答案为:H2O分子之间存在氢键;
(5)二氧化碳与过氧化钠反应生成碳酸钠与氧气,化学反应方程式为:2Na2O2+CO2=2Na2CO3+O2,
故答案为:2Na2O2+CO2=2Na2CO3+O2.
点评 本题考查结构性质位置关系应用,侧重对化学用语的考查,比较基础,注意对基础知识的积累掌握.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
1.下列有机物相关描述不正确的( )
| A. | 按照有机物系统命名法,化合物 的名称为:3,3-二乙基戊烷 的名称为:3,3-二乙基戊烷 | |
| B. | 甲醇、乙二醇、丙三醇都为饱和醇,熔沸点依次递增 | |
| C. | 甘氨酸H2N-CH2COOH、丙氨酸CH3CH(NH2)COOH、谷氨酸HOOCCH2CH2CH(NH2)COOH一定条件下形成链状三肽的结构最多有33种 | |
| D. | 分子式为C5H10O2的所有酯类的同分异构体共有9种 |
2.电负性差值为零时,可形成( )
| A. | 极性共价键 | B. | 非极性共价键 | C. | 金属键 | D. | 离子键 |
19.关于乙烯基乙炔(CH≡C-CH═CH2)分子的说法错误的是( )
| A. | 能使酸性KMnO4溶液褪色 | |
| B. | 乙烯基乙炔能与Br2发生加成反应 | |
| C. | 乙烯基乙炔分子内含有两种官能团 | |
| D. | 等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同 |
6.一定条件下,可逆反应2X(g)+3Y(g)?4Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.2mol•L-1、0.3mol•L-1、0.16mol•L-1,则下列判断不合理的是( )
| A. | 平衡时,Y和Z的生成速率之比为3:4 | |
| B. | c1的取值范围为0<c1<0.28 mol•L-1 | |
| C. | 当反应达到平衡时,扩大容器的体积,平衡会发生移动 | |
| D. | 此反应,若起始通入2 mol•L-1的X和3 mol•L-1的Y达到平衡时,与起始只通入4 mol•L-1的Z达到平衡时,各物质的组成含量不相同 |
16.已知化学反应C(s)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$CO2(g)、2CO(g)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$2CO2(g)都是放热反应,据此判断,下列说法错误的是( )
| A. | 12gC所具有的能量一定高于28gCO所具有的能量 | |
| B. | 56gCO和32gO2所具有的总能量大于44gCO2所具有的总能量 | |
| C. | 12gC和32gO2所具有的总能量大于44gCO2所具有的总能量 | |
| D. | 将一定质量的碳燃烧,生成CO2比生成CO时放出的热量多 |
15.下列说法正确的是( )
| A. | PH3比NH3稳定 | |
| B. | S2-半径比Cl-的小 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na强 | |
| D. | 把钾放入氯化钠的水溶液中可制得金属钠 |