题目内容
【题目】从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
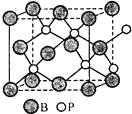
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是______(填字母序号)。
a. Fe b. FeO c. Fe3O4 d. Fe2O3
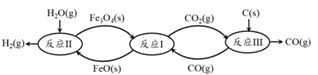
(2) 现代利用铁的氧化物循环裂解水制氢气的过程如下图所示。 整个过程与温度密切相关, 当温度低于 570℃时,反应Fe3O4(s)+4 CO(g)![]() 3Fe(s)+4 CO2(g),阻碍循环反应的进行。
3Fe(s)+4 CO2(g),阻碍循环反应的进行。
① 已知:Fe3O4(s) + CO(g) ![]() 3FeO(s) +CO2(g) ΔH1 = +19.3 kJ·mol-1
3FeO(s) +CO2(g) ΔH1 = +19.3 kJ·mol-1
3FeO(s) + H2O(g)![]() Fe3O4(s) + H2(g) ΔH2 =-57.2 kJ·mol-1
Fe3O4(s) + H2(g) ΔH2 =-57.2 kJ·mol-1
C(s)+CO2![]() 2CO(g) ΔH3 =+172.4 kJ·mol-1 。
2CO(g) ΔH3 =+172.4 kJ·mol-1 。
铁氧化物循环裂解水制氢气总反应的热化学方程式是_________。
② 下图表示其他条件一定时, Fe3O4(s)和 CO(g)反应达平衡时 CO(g)的体积百分含量随温度的变化关系。
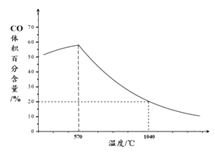
i. 当温度低于570℃时,温度降低CO的转化率____(填“增大”、“减小”或“不变”),理由是______。
ii. 当温度高于570℃时,随温度升高,反应 Fe3O4(s) + CO(g) ![]() 3FeO(s) + CO2(g)平衡常数的变化趋势是________;(填“增大”、“减小”或“不变”)1040℃时,该反应的化学平衡常数的数值是________。
3FeO(s) + CO2(g)平衡常数的变化趋势是________;(填“增大”、“减小”或“不变”)1040℃时,该反应的化学平衡常数的数值是________。
(3)① 古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应 ii 的离子方程式是_______________。
② 如今基于普鲁士蓝合成原理可检测食品中 CN-,方案如下:
![]()
若试纸变蓝则证明食品中含有 CN-,请解释检测时试纸变蓝的原因_________。
(4)已知25℃时,Kap[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配置100mL 5mol/LFeCl3溶液,为使配置过程中不出现浑浊现象,则至少需要加入2mol/L的盐酸_________mL(忽略加入盐酸体积)。
【答案】cC(s) + H2O(g) =H2(g) + CO(g) ΔH = + 134.5 kJ· mol-1增大理由:当温度低于570℃时,温度降低,CO的体积百分含量降低,可逆反应Fe3O4+4CO(g)![]() 3Fe(s)+4CO2(g) 正向移动,故CO的转化率增大增大43[Fe(CN)6]4- + 4Fe3+ =Fe4[Fe(CN)6]3↓碱性条件下,Fe2+与 CN-结合生成[Fe(CN)6]4- ,Fe2+被空气中 O2 氧化生成 Fe3+ ,[Fe(CN)6]4- 与 Fe3+反应生成普鲁士蓝使试纸显蓝色2.5
3Fe(s)+4CO2(g) 正向移动,故CO的转化率增大增大43[Fe(CN)6]4- + 4Fe3+ =Fe4[Fe(CN)6]3↓碱性条件下,Fe2+与 CN-结合生成[Fe(CN)6]4- ,Fe2+被空气中 O2 氧化生成 Fe3+ ,[Fe(CN)6]4- 与 Fe3+反应生成普鲁士蓝使试纸显蓝色2.5
【解析】(1)古代中国四大发明之一的司南是由天然磁石制成的,磁铁成分主要是四氧化三铁,选c;
(2)①Ⅰ.Fe3O4(s)+CO(g)3FeO(s)+CO2(g)△H1═+19.3kJmol-1
Ⅱ.3FeO(s)+H2O(g)Fe3O4(s)+H2(g)△H2═-57.2kJmol-1
Ⅲ.C(s)+CO2(g)2CO(g)△H3═+172.4kJmol-1
依据盖斯定律计算Ⅰ+Ⅱ+Ⅲ得到铁氧化物循环裂解水制氢气总反应的热化学方程式;C(s)+H2O(g)═H2(g)+CO(g)△H═+134.5kJmol-1 ;
②i. 当温度低于570℃时,温度降低CO的转化率增大;因为当温度低于570℃时,温度降低,CO的体积百分含量降低,可逆反应Fe3O4+4CO(g)![]() 3Fe(s)+4CO2(g) 正向移动,故CO的转化率增大。
3Fe(s)+4CO2(g) 正向移动,故CO的转化率增大。
ii.高于570°C,随温度升高,反应Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g)平衡正向进行,平衡常数的变化趋势增大,1040℃时CO体积分数为20%,结合三行计算列式计算得到平衡浓度,设起始浓度CO为1mol/L,消耗CO浓度为x
3FeO(s)+CO2(g)平衡正向进行,平衡常数的变化趋势增大,1040℃时CO体积分数为20%,结合三行计算列式计算得到平衡浓度,设起始浓度CO为1mol/L,消耗CO浓度为x
Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g)
3FeO(s)+CO2(g)
起始量(mol/L) 1 0
变化量(mol/L) xx
平衡量(mol/L) 1-x x![]() =20%,x=0.8mol/L,K=
=20%,x=0.8mol/L,K=![]() =4;
=4;
(3)①[Fe(CN)6]4-和Fe3+反应生成Fe4[Fe(CN)6]3蓝色沉淀,反应的离子方程式为:3[Fe(CN)6]4-+4Fe3+═Fe4[Fe(CN)6]3↓;
②基于普鲁士蓝合成原理可检测食品中CN-,碱性条件下,Fe2+与CN-结合生成[Fe(CN)6]4-;Fe2+被空气中O2氧化生成Fe3+;[Fe(CN)6]4-与Fe3+反应生成普鲁士蓝使试纸显蓝色。
(4)若不出现浑浊现象,则c(Fe3+)×C3(OH-)≤Ksp[Fe(OH)3],代入有关数据后可求出c(OH-)≤2×10-13mol/L,c(H+)≥0.05mol/L,则加入盐酸的体积至少为![]() =0.0025L=2.5mL。
=0.0025L=2.5mL。

【题目】某实验小组欲用酸性KMnO4和H2C2O4反应通过测定单位时间内生成 CO2的量来探究影响反应速率的因素,设计实验方案如下:
实验序号 | A 溶液 | B 溶液 |
① | 20 mL 0.1 molL-1 H2C2O4 溶液 | 30 mL 0.01 molL-1 KMnO4 酸性溶液 |
② | 20 mL 0.2 molL-1 H2C2O4 溶液 | 30 mL 0.01 molL-1 KMnO4 酸性溶液 |

(1)检验上图装置气密性的最简便方法为:____________。
(2)H2C2O4溶液与酸性 KMnO4溶液反应的化学方程式为____________。
(3)该实验探究的是___________因素对化学反应速率的影响,相同时间内针筒中所得CO2的体积大小关系是___________(填实验序号)。
(4)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=________(若忽略溶液混合前后体积的变化)。
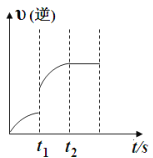
(5)小组同学发现反应速率总是如上右图所示,积极探究t1~t2时间内速率变快的主要原因,提出假设可能是:①__________、②_________、③K+对该反应有催化作用。