题目内容
【题目】某实验小组欲用酸性KMnO4和H2C2O4反应通过测定单位时间内生成 CO2的量来探究影响反应速率的因素,设计实验方案如下:
实验序号 | A 溶液 | B 溶液 |
① | 20 mL 0.1 molL-1 H2C2O4 溶液 | 30 mL 0.01 molL-1 KMnO4 酸性溶液 |
② | 20 mL 0.2 molL-1 H2C2O4 溶液 | 30 mL 0.01 molL-1 KMnO4 酸性溶液 |

(1)检验上图装置气密性的最简便方法为:____________。
(2)H2C2O4溶液与酸性 KMnO4溶液反应的化学方程式为____________。
(3)该实验探究的是___________因素对化学反应速率的影响,相同时间内针筒中所得CO2的体积大小关系是___________(填实验序号)。
(4)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=________(若忽略溶液混合前后体积的变化)。
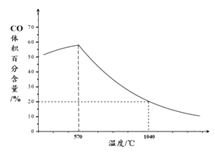
(5)小组同学发现反应速率总是如上右图所示,积极探究t1~t2时间内速率变快的主要原因,提出假设可能是:①__________、②_________、③K+对该反应有催化作用。
【答案】
(1)先关闭分液漏斗的活塞,再轻轻向外拉(或向内压)注射器的活塞,松手后恢复原位,表明气密性良好。
(2)2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
(3)浓度;②>①
(4)0.0052mol/L
(5)该反应为放热反应;反应生成的Mn2+对该反应有催化作用
【解析】
试题分析:(1)检验该装置气密性最简单的方法是:先关闭分液漏斗的活塞,再轻轻向外拉(或向内压)注射器的活塞,松手后恢复原位,表明气密性良好。
(2)酸性高锰酸钾溶液中含有硫酸,H2C2O4溶液与酸性 KMnO4溶液反应生成二氧化碳、硫酸锰、硫酸钾和水,配平后可得该反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4= K2SO4+2MnSO4 + 10CO2 ↑+ 8H2O。
(3)对比①②实验可探究浓度对化学反应速率的影响,②中A溶液的浓度比①中大,化学反应速率大,所得CO2的体积大。
(4)CO2的物质的量是:4.48mL×10-322.4mol/l=0.0002mol,设2min末,反应(MnO4-)为X
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
2 10
X 0.0002mol
解得 X=0.00004mol,
30mL×10-3×0.01molL-1-0.00004mol=0.00026mol
C(MnO4-)=nv=0.00026mol0.05L=0.0052mol/L
故答案为:0.0052mol/L;
(5)温度升高,化学反应速率加快,若该反应为放热反应,则速率变化与图像相符;催化剂能加快化学反应的速率,产物Mn2+(或MnSO4)是反应的催化剂。