题目内容
(15分)某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质。某化学课外小组设计以下流程,取该矿样为原料生产CuC12·2H2O 晶体。
已知:常温下,金属离子开始沉淀和沉淀完全时的pH 见下表。
回答下列问题:

(l)步骤①的焙烧过程中需要通入氧气。在实验室中,可使用常见化学物质利用上图所示装置制取氧气,试写出熟悉的符合上述条件的两个化学方程式:______________________、______________________。
(2)焙烧产生的尾气中含有的一种气体是形成酸雨的污染物,若将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:____________________、__________________。
(3)步骤②酸浸过程中,需要用到3 mol · L-1的盐酸100 mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有_______________________________________。
(4)步骤④加入物质X的目的是_________________________________________,物质X 可以选用下列物质中的______________________。
(A)氢氧化钠 (B)稀盐酸 (C)氨水 (D)氧化铜
(5)当溶液中金属离子浓度低于1×10-5 mol · L-1时,认为该金属离子沉淀完全,则Ksp[Fe(OH)2]=_____。

已知:常温下,金属离子开始沉淀和沉淀完全时的pH 见下表。
| 金属离子 | 氢氧化物开始沉淀的pH | 氢氧化物沉淀完全的pH |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |

(l)步骤①的焙烧过程中需要通入氧气。在实验室中,可使用常见化学物质利用上图所示装置制取氧气,试写出熟悉的符合上述条件的两个化学方程式:______________________、______________________。
(2)焙烧产生的尾气中含有的一种气体是形成酸雨的污染物,若将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:____________________、__________________。
(3)步骤②酸浸过程中,需要用到3 mol · L-1的盐酸100 mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有_______________________________________。
(4)步骤④加入物质X的目的是_________________________________________,物质X 可以选用下列物质中的______________________。
(A)氢氧化钠 (B)稀盐酸 (C)氨水 (D)氧化铜
(5)当溶液中金属离子浓度低于1×10-5 mol · L-1时,认为该金属离子沉淀完全,则Ksp[Fe(OH)2]=_____。
(1)2H2O2 ="==" 2H2O + O2 ↑,2Na2O2 + 2H2O ="==" 4NaOH + O2 ↑。
(2)2H2SO3+O2=2H2SO4,2(NH4)2SO3+O2=2(NH4)2SO4,2NH4HSO3+O2=2NH4HSO4
(3)100 mL容量瓶、量筒。
(4)调控溶液的pH,使Fe3+以Fe(OH)3沉淀的形式析出,D。
(5)1×10-15。
(2)2H2SO3+O2=2H2SO4,2(NH4)2SO3+O2=2(NH4)2SO4,2NH4HSO3+O2=2NH4HSO4
(3)100 mL容量瓶、量筒。
(4)调控溶液的pH,使Fe3+以Fe(OH)3沉淀的形式析出,D。
(5)1×10-15。
试题分析:(1)根据装置图可知是固液不加热制气体,所以用H2O2和Na2O2来制取O2反应方程式为:2H2O2 ="==" 2H2O + O2 ↑,2Na2O2 + 2H2O ="==" 4NaOH + O2 ↑。(2)尾气中含有的是SO2,SO2没有强氧化性不能与NH3反生氧化还原反应,SO2有较强的还原性,可以被空气中的O2所氧化,所以可能发生的氧化还原反应为2H2SO3+O2=2H2SO4,2(NH4)2SO3+O2=2(NH4)2SO4,2NH4HSO3+O2=2NH4HSO4(3)配制3mol · L-1的盐酸100 mL除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有100 mL容量瓶、量筒。(4)根据氢氧化物开始沉淀和完全沉淀的pH可知,只要调节pH值,就可以Fe3+以Fe(OH)3沉淀的形式析出,达到除杂的目的。为了不引入新杂质,还能调节pH值,所以选铜的难溶物,如CuO、Cu(OH)2、CuCO3等。(5)Fe(OH)2完全沉淀的pH是9.0,所以Ksp[Fe(OH)2]=c(Fe2+)·c2(OH-)=1×10-5×(1×10-5)2=1×10-15。
点评:本题属于实验与理论的结合,难度适中,高考中的热门题。

练习册系列答案
相关题目
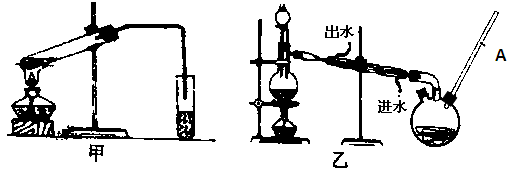

 水解液
水解液 中和液
中和液 溶液变蓝
溶液变蓝 无红色沉淀
无红色沉淀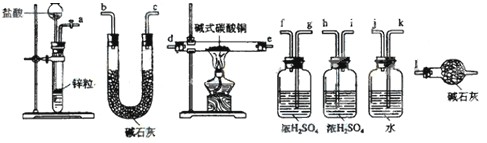
 溶液中。
溶液中。 在浓硝酸中的钝化
在浓硝酸中的钝化 移液管吸取市售食醋
移液管吸取市售食醋 容量瓶中,加水稀释至刻度线,摇匀得待测食醋溶液
容量瓶中,加水稀释至刻度线,摇匀得待测食醋溶液