题目内容
【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由软锰矿浆(主要成分是MnO2)吸收含硫废渣产生的废气制备,工艺如下图所示。
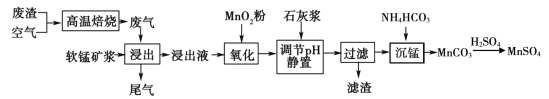
已知:浸出液的pH <2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。请回答下列问题:
(l)高温焙烧前需将矿石研成粉末,其目的是____。
(2)“氧化”中添加适量的MnO2的作用是____(用离子方程式表示);写出“沉锰”的离子方程式____。
(3)下列各组试剂中,能准确测定尾气中SO2含量的是____。(填编号)
a NaOH溶液、酚酞试液
b 稀H2SO4酸化的KMnO4溶液
c 碘水、淀粉溶液
d 氨水、酚酞试液
(4)滤渣的主要成分有____。
(5)若要从MnSO4溶液中得到高纯硫酸锰必须进行的实验操作顺序是____(用字母填空)。
a 过滤洗涤 b 蒸发浓缩 c 冷却结晶 d 干燥
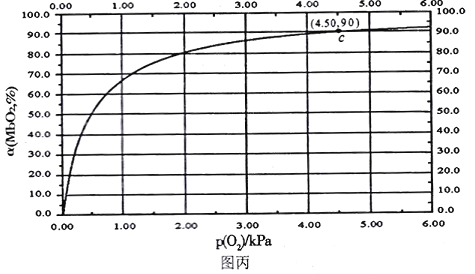
(6)已知:![]() pH =7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10 -6mol/L),需调节溶液pH范围为____
pH =7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度均小于1×10 -6mol/L),需调节溶液pH范围为____
【答案】增大反应物接触面积,加快反应速率并使其充分燃烧,提高原料利用率 将Fe2+氧化为Fe3+ Mn2++2HCO3=MnCO3↓+CO2↑+H2O b、c 氢氧化铁、氢氧化铝 bcad 5.0<pH<7.1
【解析】
高温焙烧含硫废渣产生的SO2废气,软锰矿浆的主要成分是MnO2,通入SO2浸出液的pH<2,其中的金属离子主要是Mn2+,则MnO2与SO2发生氧化还原反应,浸出液还含有少量的Fe2+、Al3+等其他金属离子,Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+,在氧化后的液体中加入石灰浆,调节pH值,Fe3+、Al3+阳离子通过调pH值,转化为氢氧化铁、氢氧化铝沉淀,过滤,滤渣主要有氢氧化铁、氢氧化铝,最后向滤液中加入碳酸氢铵的到碳酸锰沉淀,用稀硫酸溶解沉淀得到硫酸锰。
(l)高温焙烧前需将矿石研成粉末,可增大与空气的接触面积,使废渣充分燃烧,加快反应速率,同时也可提高原料利用率;
(2) “氧化”中添加适量的MnO2的作用是将Fe2+氧化为Fe3+;根据分析和流程,沉锰的反应为:Mn2++2HCO3=MnCO3↓+CO2↑+H2O;
(3)a.二氧化硫和氢氧化钠反应生成亚硫酸钠,亚硫酸钠和二氧化硫、水又能反应生成亚硫酸氢钠,有两步反应,所以无法准确测定尾气中SO2含量,故a错误;
b.稀H2SO4酸化的KMnO4溶液和二氧化硫能发生氧化还原反应而使溶液褪色,只发生一步反应,所以能准确测定尾气中SO2含量,故b正确;
c.碘和二氧化硫能发生氧化还原反应而使溶液褪色,只发生一步反应,所以能准确测定尾气中SO2含量,故c正确;
d.氨水和二氧化硫反应生成亚硫酸铵,亚硫酸铵和二氧化硫和水又能反应生成亚硫酸氢铵,有两步反应,所以无法准确测定尾气中SO2含量,故d错误;
故答案为b、c;
(4)Fe3+、Al3+阳离子通过调pH值,转化为氢氧化铁、氢氧化铝沉淀,同时生成微溶的硫酸钙,所以滤渣主要有氢氧化铁、氢氧化铝;
(5)除杂后,若要从MnSO4溶液中得到高纯硫酸锰必须进行的实验操作是蒸发浓缩、冷却结晶、过滤洗涤、干燥,故操作顺序为bcad;
(6)pH=7.1时Mn(OH)2开始沉淀,室温下,除去MnSO4溶液中的Fe3+、Al3+,氢氧化铝完全变成沉淀时的pH:Ksp[Al(OH)3]=1×10-33=c(Al3+)×c3(OH-),c(Al3+)=1×10-6mol·L-1,解得:c(OH-)=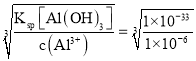 =1×10-9mol·L-1,c(H+)=
=1×10-9mol·L-1,c(H+)=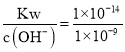 =1×10-5mol·L-1,pH=5,同理Fe(OH)3完全变成沉淀时的pH:Ksp[Fe(OH)3]=3×10-39= c(Fe 3+)×c3(OH-),c(OH-)=
=1×10-5mol·L-1,pH=5,同理Fe(OH)3完全变成沉淀时的pH:Ksp[Fe(OH)3]=3×10-39= c(Fe 3+)×c3(OH-),c(OH-)=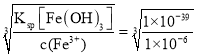 =1×10-11mol·L-1,c(H+)=
=1×10-11mol·L-1,c(H+)=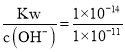 =1×10-3mol·L-1,pH=3,故要使Fe3+、Al3+全部沉淀,调节pH范围是:5.0<pH<7.1。
=1×10-3mol·L-1,pH=3,故要使Fe3+、Al3+全部沉淀,调节pH范围是:5.0<pH<7.1。

【题目】某化学兴趣小组设计实验制备苯甲酸异丙酯,其原理为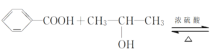
![]() ,用如图所示装置进行实验:
,用如图所示装置进行实验:
物质的部分物理性质如表所示:
物质 | 相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 水溶性 |
苯甲酸 | 122 | 1.27 | 249 | 微溶 |
异丙醇 | 60 | 0.79 | 82 | 易溶 |
苯甲酸异丙酯 | 164 | 1.17 | 218 | 不溶 |
实验步骤:
步骤Ⅰ.在干燥的仪器a中加入38.1g苯甲酸、30mL异丙醇和15mL浓硫酸,再加入几粒沸石;
步骤Ⅱ.加热至70℃左右,保持恒温半小时;
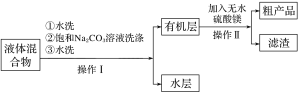
步骤Ⅲ.将仪器a中液体进行如下所示操作得到粗产品:
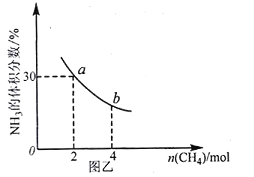
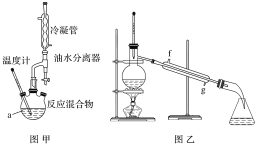
步骤Ⅳ.将粗产品用图乙所示装置进行精制。
试回答下列问题:
(1)步骤Ⅰ中加入三种试剂的先后顺序一定错误的是___(填字母)。
A.异丙醇、苯甲酸、浓硫酸
B.浓硫酸、异丙醇、苯甲酸
C.异丙醇、浓硫酸、苯甲酸
(2)图甲中仪器a的名称为___。加入的苯甲酸和异丙醇中,一般使异丙醇稍过量,目的是___。
(3)本实验一般采用水浴加热,因为温度过高会使产率___(填“增大”“减小”或“不变”)。
(4)步骤III的操作Ⅰ中第二次水洗的目的是__,操作Ⅱ中加入无水硫酸镁的作用为___。
(5)步骤Ⅳ操作时应收集218℃的馏分,如果温度计水银球偏上,则收集的精制产品中可能混有的杂质为___(填物质名称)。
(6)如果得到的苯甲酸异丙酯的质量为40.930g,则该实验的产率为___%(结果保留2位有效数字)。
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请回答下列问题:
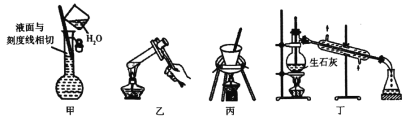
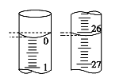
(1)观察图,标准液盐酸应放入__滴定管中。(填“甲”或“乙”)

(2)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视__,滴定终点的现象为__。
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为__mL,所用盐酸溶液的体积为___mL。
(4)某学生根据3次实验分别记录有关数据如表所示:
滴定次数 | 待测NaOH溶液的体积 | 0.1000mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据表中数据计算该NaOH溶液的物质的量浓度__。
(5)下列操作中可能使所测NaOH溶液的浓度数值偏低的是__(填字母序号)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数