题目内容
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请回答下列问题:
(1)观察图,标准液盐酸应放入__滴定管中。(填“甲”或“乙”)

(2)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视__,滴定终点的现象为__。
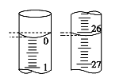
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为__mL,所用盐酸溶液的体积为___mL。
(4)某学生根据3次实验分别记录有关数据如表所示:
滴定次数 | 待测NaOH溶液的体积 | 0.1000mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据表中数据计算该NaOH溶液的物质的量浓度__。
(5)下列操作中可能使所测NaOH溶液的浓度数值偏低的是__(填字母序号)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
【答案】甲 溶液中颜色变化 当滴入最后一滴HCl溶液,颜色由黄色变为红色,且30s内不恢复 0.00 26.10 0.1044mol/L D
【解析】
酸碱中和滴定的计算中,一般取三次滴定的数据的平均值计算,但此题中,第二次数据明显异常,要舍去;滴定中的误差分析,要根据公式![]() 来分析,其中
来分析,其中![]() 和
和![]() 是定值,
是定值,![]() 与
与![]() 成正比。
成正比。
(1)标准液盐酸应放入酸式滴定管中,甲为酸式滴定管,故答案为:甲;
(2)滴定时,眼睛注视锥形瓶中颜色变化,滴定终点的现象为:当滴入最后一滴HCl溶液,颜色由黄色变为红色,且30s内不恢复,故答案为:液面颜色;当滴入最后一滴HCl溶液,颜色由黄色变为红色,且30s内不恢复;
(3)酸式滴定管读数时,视线要与凹液面的最低处保持水平,所取液体为二次读数之差,第一次读数为:0.00 mL,第二次读数为:26.10 mL,故答案为:0.00;26.10;
(4)根据公式,![]() ,
,![]() ,故答案为:0.1044mol/L;
,故答案为:0.1044mol/L;
(5)根据公式![]()
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸,使标准酸的浓度变小,![]() 增大,NaOH溶液的浓度偏大,A不符合;
增大,NaOH溶液的浓度偏大,A不符合;
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥,对待测液的物质的量无影响,故![]() 不变,NaOH溶液的浓度无影响,B不符合;
不变,NaOH溶液的浓度无影响,B不符合;
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,![]() 增大,NaOH溶液的浓度偏大,C不符合;
增大,NaOH溶液的浓度偏大,C不符合;
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数,![]() 减小,NaOH溶液的浓度偏小,D符合,答案为:D。
减小,NaOH溶液的浓度偏小,D符合,答案为:D。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】经测定乙醇的分子式是C2H6O,由于有机化合物普遍存在同分异构现象,推测乙醇分子的结构可能是下列两种之一:
Ⅰ.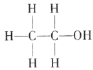 Ⅱ.
Ⅱ.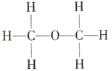
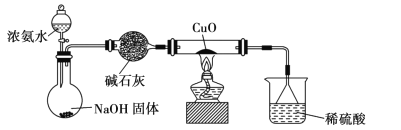
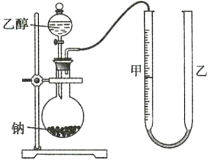
为确定其结构,应利用物质的特殊性质进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,甲、乙、丙三名学生利用如图所示装置进行实验确定乙醇分子的结构。图中量气装置由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~200mL),供量气用;乙管可上下移动,以调节液面高低。
(1)学生甲得到一组实验数据;
乙醇的物质的量 | 氢气的体积(标准状况下) |
0.01mol | 0.112L |
根据以上数据推断,乙醇的结构应为___(填“Ⅰ”或“Ⅱ”),原因是___。
(2)学生乙认为:为了较准确地测量氢气的体积,除了必须检查整个装置的气密性外,在读取反应前后甲管中液面读数的过程中,应注意___(填序号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
(3)学生丙不想通过称取乙醇的质量来确定乙醇的物质的量,那么他还需要知道的数据是___。