题目内容
1.下列说法不正确的是( )| A. | 轮船底部焊上锌块可减级船体腐蚀,这种方法称为粞牲阳极的阴极保护法 | |
| B. | 精炼铜时,与电源负极相连的是纯铜,电极反应式为:Cu2++2e-═Cu | |
| C. | 镀层破损后,镀锌铁板比镀锡铁板更耐腐蚀 | |
| D. | 恒温下,用惰性电极电解饱和Na2CO3溶液,溶液浓度变大,有晶体析出 |
分析 A、在原电池中,负极上的金属易被腐蚀,正极上的金属被保护;
B、根据电解精炼铜的原理以及电解池的工作原理来回答;
C、铁、锡和合适的电解质溶液构成的原电池中,铁作负极,易被腐蚀,锌、铁和合适的电解质溶液构成的原电池中,锌作负极,铁作正极被保护;
D、盛有饱和碳酸钠溶液的烧杯中插入惰性电极,保持温度不变,通电时氢离子放电生成氢气,氢氧根离子放电生成氧气,即电解水,结合饱和溶液溶剂减少来解答.
解答 解:A、在轮船外壳焊上金属锌,可以保护金属锌,这是牺牲阳极的阴极保护法,故A正确;
B、精炼铜时,粗铜做阳极,金属锌、铁先于铜失电子,纯铜做阴极,电极反应式为:Cu2++2e-═Cu,故B正确;
C、镀层破损后,镀锡铁板中铁加快腐蚀,镀锌铁板中铁被保护,所以镀锌铁板比镀锡铁板更耐腐蚀,故C正确;
D、盛有饱和碳酸钠溶液的烧杯中插入惰性电极,保持温度不变,通电时氢离子放电生成氢气,氢氧根离子放电生成氧气,即电解水,因温度不变,溶剂减少后还是饱和溶液,则溶液浓度不变,有晶体析出,故D错误;
故选D.
点评 本题考查了原电池原理、电解池原理及金属的腐蚀与防护,易错选项是D,注意用惰性电极电解饱和碳酸钠时,实则电解的是水,溶液中的溶质不变而溶剂改变,导致溶液的浓度改变.

练习册系列答案
相关题目
11.下列物质熔沸点最高的是( )
| A. | 甲烷 | B. | 正丁烷 | C. | 异丁烷 | D. | 丙烷 |
9.下列实验现象能说明SO2具有漂白性质的是( )
| A. | 将SO2通入溴水,溴水褪色 | |
| B. | 将SO2气体通入滴入有酚酞的NaOH溶液中,红色褪色 | |
| C. | 将SO2通入品红溶液中,品红溶液褪色 | |
| D. | 将SO2通入酸性高锰酸钾溶液中,溶液褪色 |
16.一定温度下,反应N2(g)+O2(g)═2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
| A. | 缩小容器的体积使压强增大 | B. | 体积不变,充入N2 | ||
| C. | 恒容,充入He | D. | 降低反应温度 |
6.下列分子式表示的物质一定是纯净物的是( )
| A. | C2H60 | B. | C7H8O | C. | CH4O | D. | C2H4Cl2 |
13.下列各组微粒均为正四面体结构,且仅含极性键的是( )
| A. | C2H2、BeCl2 | B. | SiCl4、NH4+ | C. | H2S、P4 | D. | CH4、BF3 |
7. 的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )
的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )
 的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )
的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
8.下列物质中含有共价键的离子化合物是( )
| A. | KOH | B. | MgCl2 | C. | CO2 | D. | CH4 |

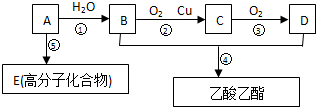
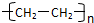

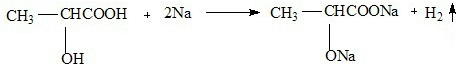 .
.