��Ŀ����
12���ʻ���COS������Ϊһ����ʳѬ�������ܷ�ֹijЩ���桢�߳�������Σ�����ں����ܱ������У���CO��H2S��ϼ��Ȳ��ﵽ����ƽ�⣺CO��g��+H2S��g��?COS��g��+H2��g�� K=0.1
��ӦǰCO�����ʵ���Ϊ10mol��ƽ���CO���ʵ���Ϊ8mol������˵����ȷ���ǣ�������
| A�� | �����¶ȣ�H2SŨ�����ӣ������÷�Ӧ�����ȷ�Ӧ | |
| B�� | ͨ��CO������Ӧ���������� | |
| C�� | ��ӦǰH2S���ʵ���Ϊ7mol | |
| D�� | CO��ƽ��ת����Ϊ80% |
���� A�������¶ȣ�H2SŨ�����ӣ�˵��ƽ�������ƶ��������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ���
B��ͨ��CO������Ӧ����˲����������С��
C����ӦǰCO�����ʵ���Ϊ10mol��ƽ���CO���ʵ���Ϊ8mol���跴ӦǰH2S���ʵ���Ϊn����
CO��g��+H2S��g��?COS��g��+H2��g�� ��ʼ��mol����10 n 0 0
�仯��mol����2 2 2 2
ƽ�⣨mol����8 n-2 2 2
��Ӧǡ�����������Ŀ���䣬�������ʵ�������Ũ�ȴ���ƽ�ⳣ������ʽK=$\frac{c��COS����c��{H}_{2}��}{c��CO����c��{H}_{2}S��}$�з��̼��㣻
D������C�еļ������ݼ���CO��ƽ��ת���ʣ�
��� �⣺A�������¶ȣ�H2SŨ�����ӣ�˵��ƽ�������ƶ��������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����÷�Ӧ�Ƿ��ȷ�Ӧ����A����
B��ͨ��CO������Ӧ����˲����������С����B����
C����ӦǰCO�����ʵ���Ϊ10mol��ƽ���CO���ʵ���Ϊ8mol���跴ӦǰH2S���ʵ���Ϊn����
CO��g��+H2S��g��?COS��g��+H2��g��
��ʼ��mol����10 n 0 0
�仯��mol����2 2 2 2
ƽ�⣨mol����8 n-2 2 2
��Ӧǡ�����������Ŀ���䣬�����������ʵ�������Ũ�ȼ���ƽ�ⳣ������K=$\frac{c��COS����c��{H}_{2}��}{c��CO����c��{H}_{2}S��}$=$\frac{2��2}{8����n-2��}$=0.1�����n=7����C��ȷ��
D�������������ݣ���֪CO��ƽ��ת����Ϊ$\frac{2mol}{10mol}$��100%=20%����D����
��ѡC��
���� ���⿼��Ӱ�컯ѧ��Ӧ���ʵ����ء���ѧƽ�ⳣ��Ӧ�á���ѧƽ����йؼ��㣬�Ƚϻ�����ע��������������ʽ�����ⷨ�ڻ�ѧƽ������е�Ӧ�ã�

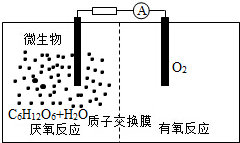 ��������ָ������������½���ѧ��ת��Ϊ���ܵ�װ�ã��乤��ԭ����ͼ��ʾ�������й������ص�˵��������ǣ�������
��������ָ������������½���ѧ��ת��Ϊ���ܵ�װ�ã��乤��ԭ����ͼ��ʾ�������й������ص�˵��������ǣ�������| A�� | ������Ӧ����CO2���� | |
| B�� | ����ٽ��˷�Ӧ�е��ӵ�ת�� | |
| C�� | ����ͨ������Ĥ�Ӹ��������������� | |
| D�� | ����ܷ�ӦΪC6H12O6+6O2�T6CO2+6H2O |
| A�� | ����Һ��Na+��NH4+��NO3-��Mg2+���Դ������� | |
| B�� | ͨ��CO2���������ɫ���� | |
| C�� | ��H2S��Ӧ�����ӷ���ʽ��Cu2++S2-=CuS�� | |
| D�� | �����Ũ��ˮ��Ӧ�����ӷ���ʽ��Cu2++2NH3•H2O=Cu��OH��2��+2NH4+ |
| A�� | I��ԭ�Ӱ뾶����Br��HI��HBr�����ȶ���ǿ | |
| B�� | P�ķǽ�����ǿ��Si��H3PO4��H2SiO3������ǿ | |
| C�� | Al2O3��MgO������NaOH��Һ��Ӧ | |
| D�� | SO2��SO3�������ͨ��Ba��NO3��2��Һ�ɵõ�BaSO3��BaSO4 |
| A�� | ������ϩ�����к�̼̼˫�� | B�� | �Ե���Ϊԭ�Ͽ���ȡ�������� | ||
| C�� | ������3��ͬ���칹�� | D�� | ��֬��������Ӧ���ڼӳɷ�Ӧ |
| A�� | Ϊ�ⶨ������ˮ��pH���ò�����պȡҺ�����pH��ֽ�ϣ������ɫ�����ռ��� | |
| B�� | ������ʵ��ʱ����������ƿ��Ӧ�����ʯ���Է����У�����ڷ���ǰ�������Ǽӷ�ʯ��Ӧ����ֹͣ���ȣ���ȴ�� | |
| C�� | ��δ֪��Һ�еμ�BaCl2��Һ���ְ�ɫ��������ϡ���ᣬ�������ܽ⣬˵����δ֪��Һ�д���SO42-��SO32- | |
| D�� | �ᴿ������������ص��Ȼ��ƣ�Ӧ�����ڽϵ��¶����Ƶ�Ũ��Һ����ȴ�ᾧ�����ˡ�����ķ��� |