题目内容
【题目】在有机化学中,硫酰氯(SO2Cl2)长用作氯化剂和氯磺化剂,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。现在拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =97.3 kJ·mol1,实验装置如图所示(部分夹持装置未画出)。
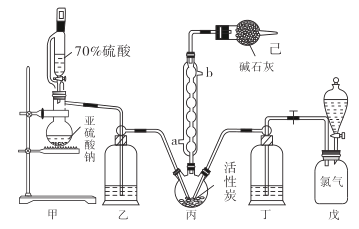
已知:硫酰氯通常条件下为无色液体,熔点54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙中作为反应容器的仪器的名称为_______,装置丙中球形冷凝管的作用是________;如何控制两种反应物体积相等:____________________________________。
(2)装置戊上方分液漏斗中最好选用下列试剂:_________________(选填字母)
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 molL-1盐酸
(3)若缺少装置己,硫酰氯(SO2Cl2)会和空气中的水反应而变质,其化学方程式是______________________________。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H![]() SO2Cl2 + H2SO4,分离两种产物的方法是_____________(选填字母)。
SO2Cl2 + H2SO4,分离两种产物的方法是_____________(选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是_________________________________(用化学方程式和必要的文字加以解释)。
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为___________。
(7)请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):___________________________。
【答案】 三颈烧瓶 冷凝回流导气 观察乙、丁导管口产生气泡的速度相等 B SO2Cl2+2H2O==H2SO4+2HCl C SO2Cl2=SO2+Cl2,分解产生少量的氯气溶解在其中 75% 取产物在干燥的环境中加热至100℃,待产物的质量不在改变时,冷却后将剩余物质加入到水中;取少量溶液加入石蕊试液,溶液变红;再取少量试液加入氯化钡溶液,产生白色沉淀,则说明产品中有硫酸
【解析】分析:用干燥的氯气和二氧化硫制备SO2Cl2,甲是用亚硫酸钠与硫酸反应制备二氧化硫,与氯气在活性炭催化作用下于丙装置内发生反应制备SO2Cl2;乙、丁盛放浓硫酸干燥气体,氯气和二氧化硫不能直接排放到空气中,用已装置中的碱石灰进行吸收。据此回答。
详解:(1)装置丙中作为反应容器的仪器,名称为三颈烧瓶;装置丙中球形冷凝管的作用是冷凝回流导气;通过调节旋塞或滴液的快慢控制气体流速,使装置乙和丁导管口产生气泡的速度相等;正确答案:三颈烧瓶;冷凝回流导气 ; 观察乙、丁导管口产生气泡的速度相等。
(2)A.蒸馏水可以溶解氯气;B.饱和食盐水溶解氯气的能力很小;C.浓氢氧化钠溶液与氯气发生反应;D.6.0 mol·L-1盐酸挥发逸出杂质气体氯化氢;正确选项B。
(3)硫酰氯(SO2Cl2)会和空气中的水反应而变质,生成硫酸和盐酸,化学方程式是:SO2Cl2+2H2O==H2SO4+2HCl;正确答案:SO2Cl2+2H2O==H2SO4+2HCl。
(4)两种产物都呈液态,且沸点差别较大,采用蒸馏方法进行分离,正确选项C。
(5)SO2Cl2=SO2+Cl2,分解产生少量的氯气溶解在其中,会导致硫酰氯会发黄;正确答案: SO2Cl2=SO2+Cl2,分解产生少量的氯气溶解在其中。
(6)若反应中消耗的氯气体积为896 mL(标准状况下),氯气的物质的量为0.04mol,根据反应SO2(g)+ Cl2(g) =SO2Cl2(l)可知,制备出的SO2Cl2的量为0.04mol,质量为0.04×135=5.4g,则硫酰氯的产率为4.05/5.4×100%=75%;正确答案:75%。
(7)由于SO2Cl2+2H2O==H2SO4+2HCl发生,所以要检验SO2Cl2中混有硫酸,就要先除去SO2Cl2,根据题给信息,进行如下操作:取产物在干燥的环境中加热至100℃,待产物的质量不在改变时,冷却后将剩余物质加入到水中;取少量溶液加入石蕊试液,溶液变红;再取少量试液加入氯化钡溶液,产生白色沉淀,则说明产品中有硫酸。正确答案:取产物在干燥的环境中加热至100℃,待产物的质量不在改变时,冷却后将剩余物质加入到水中;取少量溶液加入石蕊试液,溶液变红;再取少量试液加入氯化钡溶液,产生白色沉淀,则说明产品中有硫酸。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】对利用甲烷消除NO2污染进行研究,CH4+2NO2 ![]() N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
组别 | 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
下列说法正确的是
A. 组别①中,0~20min内,NO2的降解速率为0.0125 mol·L-1·min-1
B. 由实验数据可知实验控制的温度T12
C. 40min时,表格中T2应填的数据为0.18
D. 0~10min内,CH4的降解速率①>②