题目内容
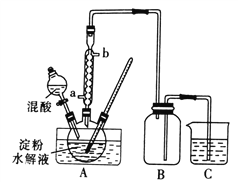
【题目】甲、乙两同学欲制取纯净的Fe(OH)2 ,根据如图所示的装置进行试验。A管中是Fe+H2SO4 , B管中是NaOH溶液,请回答下列问题。
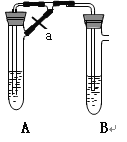
(1)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是 。
(2)同学乙:打开a,使A管中反应一段时间再 夹紧止水夹a,实验中在B管中观察到的现象是 ,B中发生反应的离子方程式为
(3)同学乙打开a的目的 ; (填甲或乙)同学可成功。
【答案】(1)在B管中观察到的现象是:生成灰白色沉淀迅速变成灰绿色,最后变成红褐色。
(2)有白色沉淀生成 Fe2++2OH-=Fe(OH)2
(3)使A管中产生的气体通入B管中赶走空气 ;乙
【解析】由于Fe(OH)2 易被空气中的氧气气氧化,所以制备它关键是隔绝氧气。
(1)先夹紧止水夹a,使A管开始反应,产生的氢气将反应液(FeCl2)压入试管B,FeCl2与NaOH溶液反应得到Fe(OH)2白色沉淀,但系统中氧气的存在会将其氧化,生成灰白色沉淀迅速变成灰绿色,最后变成红褐色
(2)打开a,使A管中反应一段时间,产生的氢气密度小,会进入试管B中,将系统中的氧气排出,再夹紧止水夹a,产生的氢气将反应液(FeCl2)压入试管B,FeCl2与NaOH溶液反应得到Fe(OH)2白色沉淀,并且可稳定存在。
(3)很明显,乙同学的制法可成功达到实验目的。

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目