题目内容
按要求写出下列方程式:
(1)实验室制取氨气
(2)雷雨天产生酸雨的最后一个方程式
(3)氯化铵受热分解
(4)氨气的催化氧化反应 .
(1)实验室制取氨气
(2)雷雨天产生酸雨的最后一个方程式
(3)氯化铵受热分解
(4)氨气的催化氧化反应
考点:化学方程式的书写
专题:
分析:(1)实验室用固体氯化铵和固体氢氧化钙反应制备氨气;
(2)雷雨天产生酸雨的最后一个反应为二氧化氮与水反应,生成硝酸和一氧化氮;
(3)氯化铵固体受热易分解为氨气和氯化氢两种气体;
(4)氨气具有还原性,氧气具有氧化性,氨气中氮元素为-3价,被氧气氧化为+2价的氮元素,所以氨气和氧气反应生成一氧化氮和水,据此分析解答.
(2)雷雨天产生酸雨的最后一个反应为二氧化氮与水反应,生成硝酸和一氧化氮;
(3)氯化铵固体受热易分解为氨气和氯化氢两种气体;
(4)氨气具有还原性,氧气具有氧化性,氨气中氮元素为-3价,被氧气氧化为+2价的氮元素,所以氨气和氧气反应生成一氧化氮和水,据此分析解答.
解答:
解:(1)铵盐和碱加热制得氨气,所以实验室常用氯化铵固体和熟石灰固体混合加热来制取氨气2NH4C1+Ca(OH)2
CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
(2)雷雨天产生酸雨发生的一系列化学反应如下:
①空气中的氮气在放电条件下与氧气直接化合,生成无色且难溶于水的一氧化氮气体;
②一氧化氮在常温下就能与空气中的氧气反应,生成红棕色的二氧化氮气体;
③二氧化氮与水反应,生成硝酸和一氧化氮;
所以雷雨天产生酸雨的最后一个反应为:3NO2+H2O=2HNO3十NO,
故答案为:3NO2+H2O=2HNO3+NO;
(3)铵盐受热易分解;氯化铵固体受热易分解为NH4Cl
NH3↑+HCl↑
故答案为:NH4Cl
NH3↑+HCl↑;
(4)NH3与过量O2在催化剂、加热条件下发生反应生成一氧化氮和水,反应方程为:4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O.
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
(2)雷雨天产生酸雨发生的一系列化学反应如下:
①空气中的氮气在放电条件下与氧气直接化合,生成无色且难溶于水的一氧化氮气体;
②一氧化氮在常温下就能与空气中的氧气反应,生成红棕色的二氧化氮气体;
③二氧化氮与水反应,生成硝酸和一氧化氮;
所以雷雨天产生酸雨的最后一个反应为:3NO2+H2O=2HNO3十NO,
故答案为:3NO2+H2O=2HNO3+NO;
(3)铵盐受热易分解;氯化铵固体受热易分解为NH4Cl
| ||
故答案为:NH4Cl
| ||
(4)NH3与过量O2在催化剂、加热条件下发生反应生成一氧化氮和水,反应方程为:4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
点评:本题考查化学方程式的书写,掌握反应原理和书写方法是解答的关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述错误的是( )
| A、使阴、阳离子结合成化合物的静电作用叫做离子键 |
| B、含共价键的化合物不一定是共价化合物 |
| C、化合物中只要含有离子键就一定属于离子化合物 |
| D、金属元素与非金属元素相化合时一定形成离子键 |
下列除杂(括号内为杂质)实验设计能达到预期目的是( )
| A、乙烷(乙烯):KMnO4酸性溶液,洗气 |
| B、乙醇(乙酸):碱石灰,蒸馏 |
| C、甲苯(苯酚):浓溴水,过滤 |
| D、溴乙烷(乙醇):苯,分液 |
下列四种物质中,既能与水发生反应,又能与碱发生反应的是( )
| A、Cl2 |
| B、CO2 |
| C、NO |
| D、SiO2 |
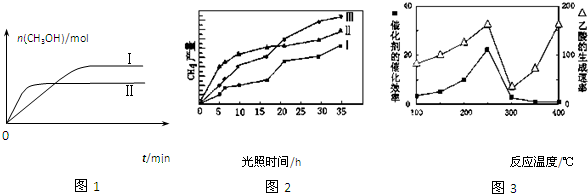
 尿素(H2NCONH2)可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)].
尿素(H2NCONH2)可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)].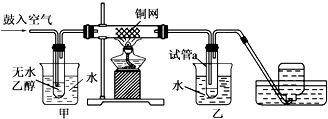
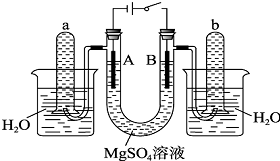 如图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色-红色,碱色-黄色)
如图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色-红色,碱色-黄色)