题目内容
【题目】在一容积不变的密闭容器中充入0.1mol/LCO2和0.1mol/LCH4 , 在一定条件下发生反应:CH4(g)+CO2(g)2CO(g)+2H2(g).测得平衡时CH4的转化率与温度、压强的关系如图.下列有关说法正确的是( ) 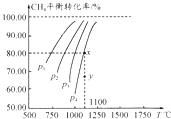
A.上述反应的△H<0
B.压强P1>P2>P3>P4
C.1100℃时该反应的平衡常数约为1.64
D.压强为P4时,y点的v正<v逆
【答案】C
【解析】解:A、从图象分析,随温度升高转化率增大,正反应吸热,△H>0,故A错误;B、压强增大,平衡向逆反应方向移动,甲烷的转化率变小,故P4>P3>P2>P1 , 故B错误;
C、反应 CH4(g)+CO2(g)2CO(g)+2H2(g),
起始(mol/L)0.1 0.1 00
变化(mol/L)0.08 0.08 0.160.16
平衡(mol/L)0.02 0.02 0.160.16
平衡常数K= ![]() =1.64,故C正确;
=1.64,故C正确;
D、在y点,甲烷的转化率小于平衡时的转化率,平衡正向移动,V正>V逆 , 故D错误.
故选C.
A、随温度的升高转化率增大;
B、增大压强,平衡向气体体积减小的方向移动;
C、利用三段式计算出平衡时的浓度求算;
D、y点时甲烷的转化率小,平衡正向移动.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目


