题目内容
20.配制100mL 0.10mol•L-1的NaOH溶液时,下列实验操作会使所配溶液浓度偏大的是( )| A. | 转移溶液时有液体飞溅 | B. | 在容量瓶中定容时俯视刻度线 | ||
| C. | 定容时凹液面最底处高于刻度线 | D. | 转移溶液后未洗涤烧杯就直接定容 |
分析 分析操作对溶质的物质的量、溶液的体积的影响,依据c=$\frac{n}{V}$可知,凡是使n偏大或者使V偏小的操作都会使浓度偏高,反正偏低,据此解答.
解答 解:A.转移溶液时有液体飞溅,导致溶质的物质的量偏小,溶液浓度偏低,故A不选;
B.在容量瓶中定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故B选;
C.定容时凹液面最底处高于刻度线,导致溶液体积偏大,溶液浓度偏低,故C不选;
D.转移溶液后未洗涤烧杯就直接定容,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故D不选;
故选:B.
点评 本题考查了一定物质的量浓度溶液的配制过程中的误差分析,明确配制原理依据c=$\frac{n}{V}$即可解答,题目难度不大.

练习册系列答案
相关题目
10.在如图点滴板上有四个溶液间反应的小实验,其对应反应的离子方程式书写错误的是( )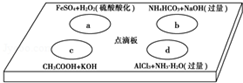

| A. | a反应:2Fe2++2H++H2O2═2Fe3++2H2O | |
| B. | b反应:NH4++OH-═NH3↑+H2O | |
| C. | c反应:CH3COOH+OH-═CH3COO-+H2O | |
| D. | d反应:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
11.现有下列两个图象:下列反应中符合两图象的是( )


| A. | H2(g)+CO(g)?C(s)+H2O(g)△H>0 | B. | 2SO3(g)?2SO2(g)+O2(g)△H>0 | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 | D. | N2(g)+3H2(g)?2NH3(g)△H<0 |
8.下列物质中主要成分为硅酸盐的是( )
| A. | 硅橡胶 | B. | 石英 | C. | 青花瓷 | D. | 金刚砂 |
15.向一定体积的0.1摩/升的醋酸溶液中加入等体积的蒸馏水后,则下列叙述正确的是( )
| A. | 溶液的pH值变小 | |
| B. | 醋酸的电离度增大 | |
| C. | 溶液的导电能力减弱 | |
| D. | 中和此溶液所需的0.1摩/升NaOH溶液的体积增加 |
5.下列物质溶于水,其电离方程式正确的是( )
| A. | NaHCO3═Na++H++CO${\;}_{3}^{2-}$ | B. | (NH4)2SO4═NH${\;}_{4}^{+}$+2SO${\;}_{4}^{2-}$ | ||
| C. | NaCl═Na++Cl- | D. | Ca(OH)2═Ca2++OH${\;}_{2}^{-}$ |
12.由硫酸钾、硫酸铝和硫酸组成的混合溶液中,c(H+)=0.2mol•L-1,c(Al3+)=0.4 mol•L-1,c( SO${\;}_{4}^{2-}$)=0.8 mol•L-1,则c(K+)为( )
| A. | 0.15 mol•L-1 | B. | 0.2 mol•L-1 | C. | 0.3 mol•L-1 | D. | 0.4 mol•L-1 |
9.下列说法正确的是( )
| A. | 自发反应在任何条件下都能实现 | |
| B. | 化学反应不一定都有能量变化 | |
| C. | 升高温度,活化分子百分数增大,化学反应速率一定增大 | |
| D. | 一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率 |
10.下列对有关概念的叙述正确的是( )
| A. | 在氧化还原反应中,氧化剂得电子还原剂失电子 | |
| B. | 胶体的微粒直径在10-100nm之间,能发生丁达尔现象 | |
| C. | 非金属氧化物为酸性氧化物,金属氧化物为碱性氧化物 | |
| D. | 能导电的物质不一定是电解质,也有可能是非电解质 |