题目内容
11.现有下列两个图象:下列反应中符合两图象的是( )
| A. | H2(g)+CO(g)?C(s)+H2O(g)△H>0 | B. | 2SO3(g)?2SO2(g)+O2(g)△H>0 | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 | D. | N2(g)+3H2(g)?2NH3(g)△H<0 |
分析 由左边的图象可知,温度越高生成物的浓度越大,说明升高温度,平衡向正反应移动,故正反应为吸热反应;
由右边图象可知,相交点左边未达平衡,相交点为平衡点,相交点右边压强增大,平衡被破坏,V逆>V正,平衡向逆反应移动,说明正反应为气体物质的量增大的反应;
综合上述分析可知,可逆反应正反应为吸热反应且正反应为气体物质的量增大的反应,据此结合选项解答.
解答 解:由左边的图象可知,温度越高生成物的浓度越大,说明升高温度,平衡向正反应移动,故正反应为吸热反应;
由右边图象可知,相交点左边未达平衡,相交点为平衡点,相交点右边压强增大,平衡被破坏,V逆>V正,平衡向逆反应移动,说明正反应为气体物质的量增大的反应;
综合上述分析可知,可逆反应正反应为吸热反应且正反应为气体物质的量增大的反应,
A.H2(g)+CO(g)?C(s)+H2O(g)△H>0,为吸热反应,但正反应是气体物质的量减小的反应,故A不符合;
B.2SO3(g)?2SO2(g)+O2(g)△H>0,为吸热反应,正反应是气体物质的量增大的反应,故B符合;
C.4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0,正反应是气体物质的量增大的反应,但为放热反应,故C不符合;
D.N2(g)+3H2(g)?2NH3(g)△H<0,为放热反应,正反应是气体物质的量减小的反应,故D不符合;
故选B.
点评 本题考查化学平衡移动图象、外界条件对化学平衡的影响等,难度不大,掌握外界条件对化学平衡的影响即可解答,注意根据图象判断可逆反应的特征.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
1.下列叙述正确的是( )
| A. | 一定温度和压强下,将 0.5mo1N2和 1.5mo1H2 置于密闭容器中充分反应生成 NH3(g),放 热 19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |||||||||
| B. | H2 标准燃烧热△H=-285.8 kJ•mol-1,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ•mol-1 | |||||||||
| C. | C(石墨)═C(金刚石)△H=+1.9kJ•mol-1,说明石墨比金刚石稳定 | |||||||||
| D. | 通常人们把拆开 1 mol 某化学键所吸收的能量看成该化学键的键能:
|
2.实验室用碳酸钠晶体配制1.00mol•L-1的Na2CO3溶液100mL,造成所配溶液浓度偏低的原因是( )
| A. | 暴露在空气中称量碳酸钠晶体(Na2CO3•10H2O)的时间太长 | |
| B. | 向容量瓶转移液体时,容量瓶事先用蒸馏水洗涤 | |
| C. | 定容时俯视刻度线 | |
| D. | 称量碳酸钠晶体(Na2CO3•10H2O)的烧杯未干燥 |
19.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1molNa2O2晶体中阴离子的个数为2NA | |
| B. | 1 mol•Lˉ1FeCl3溶液含有的Cl-数为3 NA | |
| C. | 标准状况下,2.24L苯所含的分子数为0.1NA | |
| D. | 32g O2和32g O3 所含的氧原子数都是为2NA |
6.下列化学用语正确的是( )
| A. | 氯化钠的电子式: | |
| B. | 过氧化钠的化学式:Na2O | |
| C. | Cl-的结构示意图: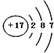 | |
| D. | 硫酸的电离方程式:H2SO4=2H++SO42- |
20.配制100mL 0.10mol•L-1的NaOH溶液时,下列实验操作会使所配溶液浓度偏大的是( )
| A. | 转移溶液时有液体飞溅 | B. | 在容量瓶中定容时俯视刻度线 | ||
| C. | 定容时凹液面最底处高于刻度线 | D. | 转移溶液后未洗涤烧杯就直接定容 |
1.由CH4和O2组成的混合气体,标准状况下的密度为1.25g•L-1,则该混合气体中CH4和O2的体积比为( )
| A. | 2:1 | B. | 1:2 | C. | 1:3 | D. | 3:2 |