题目内容
15.向一定体积的0.1摩/升的醋酸溶液中加入等体积的蒸馏水后,则下列叙述正确的是( )| A. | 溶液的pH值变小 | |
| B. | 醋酸的电离度增大 | |
| C. | 溶液的导电能力减弱 | |
| D. | 中和此溶液所需的0.1摩/升NaOH溶液的体积增加 |
分析 A.加水稀释促进醋酸电离,但溶液中氢离子浓度减小,溶液的pH增大;
B.加水稀释促进醋酸电离;
C.溶液的导电能力与离子浓度成正比;
D.中和酸需要碱的量只与酸的物质的量有关与酸的浓度无关.
解答 解:A.加水稀释促进醋酸电离,但醋酸增大的电离程度小于溶液体积增大程度,所以氢离子浓度减小,溶液的pH增大,故A错误;
B.加水稀释促进醋酸电离,则醋酸的电离度增大,故B正确;
C.溶液的导电能力与离子浓度有关,加水稀释促进醋酸电离但溶液中离子浓度减小,所以溶液的导电能力减弱,故C正确;
D.中和酸需要碱的量只与酸的物质的量有关与酸的浓度无关,所以中和此溶液所需的0.1mol•L-1 NaOH溶液的体积不变,故D错误;
故选BC.
点评 本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,知道碱中和酸只与酸的物质的量有关,与酸的强弱、浓度无关,为易错点.

练习册系列答案
相关题目
5.某Na2CO3样品中含有K2CO3、NaNO3和Ba(NO3)2三种杂质中的一种或两种.现将11g样品加入足量水中,样品全部溶解.再加入过量的CaCl2溶液,得到10g沉淀.对样品所含杂质的正确判断是( )
| A. | 肯定有NaNO3 | B. | 肯定有NaNO3,可能还含有K2CO3 | ||
| C. | 肯定没有Ba(NO3)2,可能有NaNO3 | D. | 肯定没有K2CO3和Ba(NO3)2 |
6.下列化学用语正确的是( )
| A. | 氯化钠的电子式: | |
| B. | 过氧化钠的化学式:Na2O | |
| C. | Cl-的结构示意图: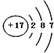 | |
| D. | 硫酸的电离方程式:H2SO4=2H++SO42- |
10.设 NA为阿伏加德罗常数的数值,下列说法中错误的是( )
| A. | 在标准状况下,22.4 L苯所含的碳原子数目为6NA | |
| B. | 常温常压下,6.2g氧化钠含有的离子数为0.3NA | |
| C. | 18 g 水所含的电子数目为10 NA | |
| D. | 3.2g O2、O3混合物中所含O原子一定是0.2NA |
20.配制100mL 0.10mol•L-1的NaOH溶液时,下列实验操作会使所配溶液浓度偏大的是( )
| A. | 转移溶液时有液体飞溅 | B. | 在容量瓶中定容时俯视刻度线 | ||
| C. | 定容时凹液面最底处高于刻度线 | D. | 转移溶液后未洗涤烧杯就直接定容 |
5.下列关于胶体的说法正确的是( )
| A. | 将可见光通过胶体出现“光路”是因为发生了光的折射 | |
| B. | 胶体能吸附阳离子或阴离子,故在电场作用下会产生电泳现象 | |
| C. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| D. | 向沸水中逐滴加入少量饱和FeCl3溶液,继续加热搅拌可制得Fe(OH)3胶体 |