题目内容
19.已知:2A(g)+B(g)═C(g)△H1;D(g)+B(g)═E(g)△H2;若A、D、混合气体1mol完全与B反应,放出热△H3,则A、D的物质的量之比是( )| A. | (△H2-△H3 ):2(△H1-△H3) | B. | (△H3-△H2 ):($\frac{△{H}_{1}}{2}$-△H3) | ||
| C. | (△H3-△H2 ):(△H3-$\frac{△{H}_{1}}{2}$) | D. | ($\frac{△{H}_{1}}{2}$-△H2 ):(△H3-△H2) |
分析 在热化学方程式中,化学反应的焓变和方程式的系数之间成正比,可以根据热化学方程式的意义设未知数来计算.
解答 解:设A的物质的量是amol,D的物质的量是bmol,则
①a+b=1
②$\frac{a}{2}$×△H1+b×△H2=△H3
由方程组解得,则A和D的物质的量之比 $\frac{a}{b}$=(△H3-△H2 ):($\frac{△{H}_{1}}{2}$-△H3),故选B.
点评 本题考查热化学方程式的意义,注意化学反应的焓变和方程式的系数之间成正比,难度不大.

练习册系列答案
相关题目
9.下列变化需要加入适当的氧化剂才能完成的是( )
| A. | CuO→CuSO4 | B. | Fe→FeCl2 | C. | H2SO4→H2 | D. | HNO3→N2 |
10.下列结论错误的是( )
①微粒半径:K+>Al3+>S2->Cl- ②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO ⑥非金属性:O>N>P>Si.
①微粒半径:K+>Al3+>S2->Cl- ②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO ⑥非金属性:O>N>P>Si.
| A. | 只有① | B. | ①③⑤ | C. | ②④⑤⑥ | D. | ①③ |
7.下列说法不正确的是( )
| A. | Al2O3用作耐火材料、Al(OH)3用作阻燃剂 | |
| B. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| C. | 碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜锡合金 | |
| D. | 盛放NaOH溶液的磨口玻璃瓶要用橡胶塞 |
14.下列各组分散系,需用丁达尔效应区分的是( )
| A. | 溶液和浊液 | B. | 胶体与胶体 | C. | 溶液与胶体 | D. | 溶液与溶液 |
11.手机芯片是一种在半导体材料上集合多种电子元器件的电路模块.下列可用作半导体材料的是( )

| A. | 铝 | B. | 硅 | C. | 碳 | D. | 铁 |
8.我国自主研制的嫦娥三号月球探测器的动力能源是太阳能电池,制造太阳能电池的主要材料是( )
| A. | 锂 | B. | 硅 | C. | 镍 | D. | 二氧化硅 |
9.下列离子方程式的写法正确的是( )
| A. | 单质钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 氢气在氯气中燃烧:H2+Cl2═2H++2Cl- | |
| C. | 小苏打治疗胃酸过多:H++HCO3-═H2O+CO2↑ | |
| D. | 用氯化铁溶液腐蚀铜箔制造印刷电路板:Fe3++Cu═Fe2++Cu2+ |
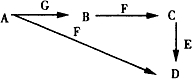 A~G为中学化学中常见的物质,B、E、F为单质,在常温下B是一种有色气体,G为黑色的固体.它们的相互转化如图所示,部分生成物未列出.试回答下列问题
A~G为中学化学中常见的物质,B、E、F为单质,在常温下B是一种有色气体,G为黑色的固体.它们的相互转化如图所示,部分生成物未列出.试回答下列问题