题目内容
【题目】已知:25℃,H2A的电离常数Kl=6.0×10-2,K2=6.0×10-5。此温度下,将1 mL浓度为0.1mol/L, 的H2A溶液加水稀释到1000mL。下列说法正确的是
A. 上述稀释过程中,H2A分子及所有离子浓度均减小
B. 上稀释过程中,![]() 的变化趋势保持增大
的变化趋势保持增大
C. 上述溶液稀释前后均存在:c(H+)=c(OH-)+2c(A2-)
D. 根据H2A的电离常数,可推知0.1mol/L NaHA溶液的pH值大于7
【答案】B
【解析】A.稀释过程中H+溶液减小,Kw不变,则OH-浓度增大,故A错误;B.稀释过程中,![]() =
=![]() ×
× =
=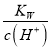 ,H+溶液减小,Kw不变,则
,H+溶液减小,Kw不变,则![]() 的变化趋势保持增大,故B正确;C.H2A是强酸,不可能完全电离,且第一步电离是主要的,溶液中c(H+)=c(OH-)+2c(A2-)+c(HA-),故C错误;D. NaHA溶液中HA-+H2O
的变化趋势保持增大,故B正确;C.H2A是强酸,不可能完全电离,且第一步电离是主要的,溶液中c(H+)=c(OH-)+2c(A2-)+c(HA-),故C错误;D. NaHA溶液中HA-+H2O![]() H2A+OH-,Kh=
H2A+OH-,Kh=![]() =
=![]() ×10-12<6.0×10-5,即在0.1mol/L NaHA溶液中HA-的水解小于其电离,溶液显酸性,溶液的pH值小大于7,故D错误;答案为B。
×10-12<6.0×10-5,即在0.1mol/L NaHA溶液中HA-的水解小于其电离,溶液显酸性,溶液的pH值小大于7,故D错误;答案为B。

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案【题目】甲酸是有机化工原料,也用作消毒剂和防腐剂,回答下列问题:
(l)以下为一些化学键的键能数据
化学键 | H-H | C=O | C-O | O-H | C-H |
键能(kJ/mol) | 436 | 728 | 326 | 464 | 414 |
合成甲酸的方法之一为CO2(g)+H2(g)![]() HCOOH(l) △H,则△H_______。
HCOOH(l) △H,则△H_______。
(2)甲酸甲酯水解制甲酸也是常见方法,而工业上可用甲醇催化脱氢制甲酸甲酯:
2 CH3OH(g)![]() HCOOCH3(g)+2H2(g) △H。已知:气体分压(P分)=气体总压(P总)×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数Kp,下图为上述反应的平衡常数Kp与温度的关系图。
HCOOCH3(g)+2H2(g) △H。已知:气体分压(P分)=气体总压(P总)×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数Kp,下图为上述反应的平衡常数Kp与温度的关系图。

① △H_______0 (填“> ”或“< ”)。
②在310℃下,将2mol 甲醇置于压强为P0的恒压密闭容器中,20分钟后到达平衡,平衡时甲醇和氢气的分压相等。计算:从开始到平衡时甲醇的平均反应速率_____mol · min-l,P0____Pa。
③ 若要进一步提高甲醇转化率,除了可以适当改变反应温度和分离出甲酸甲酯外,还可以采取的措施有_____、_______。
(3)已知常温下甲酸的电离常数K= 1.8×10-4,则pH=2甲酸的浓度约为_______。

