题目内容
9.下列离子方程式书写错误的是( )| A. | H2O2和酸性氯化亚铁溶液反应:2Fe2++H2O2+2 H+═2Fe3++2H2O | |
| B. | 碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+2Ca2++4OH-═2CaCO3↓+Mg(OH)2↓+2H2O | |
| C. | 3 mol的Cl2通入含2 mol FeI2的溶液中:2Fe2++4I-+3Cl2═2Fe3++6Cl-+2I2 | |
| D. | 将SO2通入Ca(ClO)2溶液中:Ca2++2ClO-+SO2+H2O═CaSO3+2HClO |
分析 A.H2O2与Fe2+在酸性条件下反应生成铁离子、水;
B.石灰水过量,反应生成碳酸钙、氢氧化镁和水;
C.碘离子的还原性强于二价铁离子,先氧化碘离子,剩余氯气再氧化二价铁离子;
D.次氯酸根离子具有强的氧化性,能够氧化亚硫酸根离子.
解答 解:A.H2O2与Fe2+在酸性条件下反应生成铁离子、水,反应的离子方程式为:H2O2+2Fe2++2H+=2Fe3++2H2O,故A正确;
B.碳酸氢镁溶液中加入过量石灰水,离子方程式:Mg2++2HCO3-+2Ca2++4OH-═2CaCO3↓+Mg(OH)2↓+2H2O,故B正确;
C.3 mol的Cl2通入含2 mol FeI2的溶液中,离子方程式:2Fe2++4I-+3Cl2═2Fe3++6Cl-+2I2,故C正确;
D.将少量SO2通入Ca(ClO)2溶液中,离子方程式:SO2 +3ClO-+Ca2++H2O=CaSO4↓+Cl-+2HClO,故D错误;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意反应物用量对反应的影响,题目难度不大.

练习册系列答案
相关题目
17.乙烯酮(CH2=C=O)在一定条件下,能与含活泼氢的化合物发生如下反应,其反应可表示为:CH2=C=O+HA→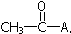 .下列各试剂,在一定条件下与乙烯酮发生反应,其产物不正确的是( )
.下列各试剂,在一定条件下与乙烯酮发生反应,其产物不正确的是( )
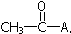 .下列各试剂,在一定条件下与乙烯酮发生反应,其产物不正确的是( )
.下列各试剂,在一定条件下与乙烯酮发生反应,其产物不正确的是( )| A. | HCl与之加成,生成CH3COCl | B. | CH3OH与之加成,生成CH3COCH2OH | ||
| C. | H2O与之加成,生成CH3COOH | D. | CH3COOH与之加成,生成 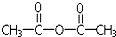 |
18.下列各项表达中正确的是( )
| A. | CS2的结构式:S=C=S | |
| B. | HCO-3的水解HCO3-+H2O?H3O++CO32- | |
| C. | 乙酸的结构简式:C2H6O2 | |
| D. | Mg2+的结构示意图: |
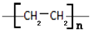 .
. CH3COOC2H5+H2O.
CH3COOC2H5+H2O.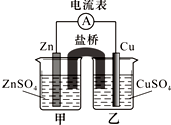 某兴趣小组为研究原电池原理设计了如下图装置,盐桥中装有含琼胶的KCl饱和溶液.
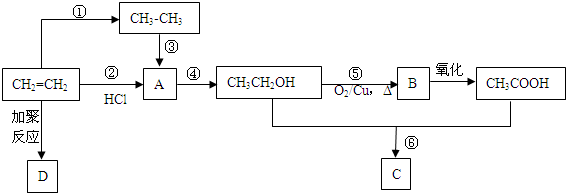
某兴趣小组为研究原电池原理设计了如下图装置,盐桥中装有含琼胶的KCl饱和溶液.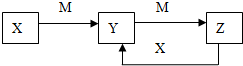 物质X、Y、Z有如图转化关系:请回答下列问题:
物质X、Y、Z有如图转化关系:请回答下列问题: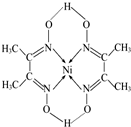 (1)第一电离能介于B、N之间的第二周期元素有3种.
(1)第一电离能介于B、N之间的第二周期元素有3种.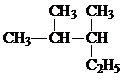 2,3-二甲基戊烷.
2,3-二甲基戊烷. 表示的分子式为C6H14;名称是2-甲基戊烷.
表示的分子式为C6H14;名称是2-甲基戊烷. 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.