题目内容
12.与50mL 0.1mol/L Na2CO3溶液中Na+的物质量浓度相同的溶液是( )| A. | 50 mL 0.1 mol/L的NaCl溶液 | B. | 100 mL 0.2 mol/L的NaCl溶液 | ||
| C. | 25 mL 0.2 mol/L的Na2SO4溶液 | D. | 10 mL 0.5 mol/L的Na2CO3溶液 |
分析 根据电解质溶液离子浓度=电解质浓度×电解质电离产生的该离子的数目.
解答 解:50mL 0.1mol•L-1 Na2CO3溶液中Na+的物质的量浓度为0.2mol/L,
A.50 mL 0.1mol•L-1的NaCl溶液中Na+的物质的量浓度为0.1mol/L,故A错误;
B.100 mL 0.2 mol•L-1的NaCl溶液中Na+的物质的量浓度为0.2mol/L,故B正确;
C.25 mL 0.2 mol•L-1的Na2SO4溶液中Na+的物质的量浓度为0.4mol/L,故C错误;
D.10 mL 0.5 mol•L-1的Na2CO3溶液中Na+的物质的量浓度为1mol/L,故D错误.
故选B.
点评 本题考查物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
3.下列事实不能用勒夏特列原理解释的是( )
| A. | 可用浓氨水和氢氧化钠固体快速制取氨气 | |
| B. | 在硫酸亚铁溶液中,加入铁粉以防止氧化变质 | |
| C. | 生产硝酸的过程中使用过量空气以提高氨气的利用率 | |
| D. | 实验室常用排饱和食盐水的方法收集氯气 |
17.取a g某铁的氧化物R溶于足量的盐酸中,加水稀释至200mL,取20mL所得溶液,向其中滴加新制的氯水,将其中的铁元素全部氧化为Fe3+,再向溶液中加入NaOH溶液使其完全沉淀,所得沉淀经过过滤、洗涤,并将沉淀灼烧至质量不再改变,称量得b g固体,则下列判断正确的是( )
| A. | 若a:b=9:1,则R的化学式为FeO | |
| B. | 若a:b=1:10,则R的化学式为Fe2O3 | |
| C. | 若a:b=29:30,则R的化学式为Fe3O4 | |
| D. | 试验过程中被还原的Cl2为(10b-a)/8mol |
1.下列哪种说法可以证明反应.N2+3H2?2NH3已达到平衡状态( )
| A. | 1个N≡N键断裂的同时,有6个H-H键断裂 | |
| B. | 1个N≡N键断裂的同时,有3个H-H键断裂 | |
| C. | 1个N≡N键断裂的同时,有6个N-H键断裂 | |
| D. | 1个N≡N键断裂的同时,有6个N-H键形成 |
2.下列化合物中,属于芳香族化合物,且属于醇类的是( )
| A. | 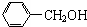 | B. |  | C. |  | D. | CH3OH |