题目内容
1.下列哪种说法可以证明反应.N2+3H2?2NH3已达到平衡状态( )| A. | 1个N≡N键断裂的同时,有6个H-H键断裂 | |
| B. | 1个N≡N键断裂的同时,有3个H-H键断裂 | |
| C. | 1个N≡N键断裂的同时,有6个N-H键断裂 | |
| D. | 1个N≡N键断裂的同时,有6个N-H键形成 |
分析 可逆反应N2(g)+3H2(g)?2NH3 (g)是反应前后气体体积减小的反应,达到平衡状态时,同一物质的正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变,据此分析解答.
解答 解:A、1个N≡N键断裂的同时,有6个H-H键断裂,都是正反应速率,无法判断是否达到平衡状态,故A错误;
B、1个N≡N键断裂的同时,有3个H-H键断裂,都是正反应速率,无法判断是否达到平衡状态,故B错误;
C、1个N≡N键断裂的同时,有6个N-H键断裂,表示正逆反应速率相等,达到了平衡状态,故C正确;
D、1个N≡N键断裂的同时,有6个N-H键形成,表示的都是正反应速率,无法判断是否达到平衡状态,故D错误;
故选C.
点评 本题考查化学平衡状态的判断,题目难度中等,注意化学平衡状态的根本标志是:①v(正) =v(逆),②各组分百分含量不变;在解题时要牢牢抓住这两个根本标志,并明确气体的颜色、密度、压强、平均相对分子质量的变化与根本标志的关系.

练习册系列答案
相关题目
12.与50mL 0.1mol/L Na2CO3溶液中Na+的物质量浓度相同的溶液是( )
| A. | 50 mL 0.1 mol/L的NaCl溶液 | B. | 100 mL 0.2 mol/L的NaCl溶液 | ||
| C. | 25 mL 0.2 mol/L的Na2SO4溶液 | D. | 10 mL 0.5 mol/L的Na2CO3溶液 |
9.下列说法正确的是( )
| A. | 硫酸工业生产过程在接触室中运用热交换技术可充分利用能源 | |
| B. | 联合制碱法生产纯碱时,先通入二氧化碳,再通入氨气 | |
| C. | 氯碱工业是以利用电解食盐水生产氯气、氢气和氢氧化钠为基础的工业体系 | |
| D. | 合成氨工业汇总,加入催化剂可提高氢气的转化率 |
16.下列各组物质中互为同分异构体的是( )
| A. | CH3CH3与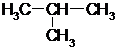 | B. | CH3CH=CH2与(环丙烷) | ||
| C. | CH3OH与HOCH2CH2OH | D. | 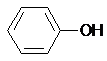 与 与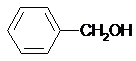 |
13.乙烷和氯气在光照条件下发生反应,生成的有机物有几种( )
| A. | 7 | B. | 8 | C. | 9 | D. | 10 |
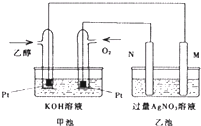 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题: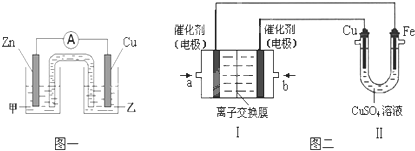
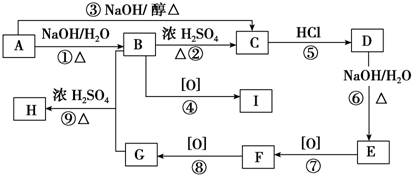
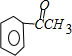 .
.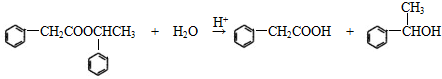 .
. .
. .
.