题目内容
15.写出下列物质的电离方程式:NaHSO4NaHSO4=Na++H++SO42-,Al2(SO4)3Al2(SO4)3=2Al3++3SO42-,NH3•H2O,NH3•H2O?NH4++OH-CH3COOHCH3COOH?CH3COO-+H+.
分析 NaHSO4是强电解质,完全电离,硫酸氢根离子应拆分;
硫酸铝是强电解质,在水溶液中或熔融状态下完全电离;
一水合氨为弱电解质,部分电离出铵根离子和氢氧根离子;
乙酸是弱电解质,在溶液中部分电离.
解答 解:NaHSO4是强酸强碱酸式盐,属强电解质,完全电离,电离出Na+、H+、SO42-离子,电离方程式为:NaHSO4=Na++H++SO42-,
硫酸铝强电解质,电离时电离出自由移动的铝离子和硫酸根离子,电离方程式为Al2(SO4)3=2Al3++3SO42-,
NH3•H2O为弱电解质,部分电离,电离方程式为NH3•H2O?NH4++OH-,
乙酸是弱电解质,在溶液中部分电离,电离时电离出自由移动的氢离子和醋酸根离子,电离方程式为:CH3COOH?CH3COO-+H+,
故答案为:NaHSO4=Na++H++SO42-;Al2(SO4)3=2Al3++3SO42-;NH3•H2O?NH4++OH-;CH3COOH?CH3COO-+H+.
点评 本题考查电离方程式的书写,难度不大,明确电解质的强弱及常见的酸根离子,并利用电荷守恒是解答关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.除去乙酸乙酯中含有的乙酸,最好的处理和操作是( )
| A. | 蒸馏 | B. | 水洗后分液 | ||
| C. | 用过量饱和碳酸钠溶液洗涤后分液 | D. | 用过量氢氧化钠溶液洗涤后分液 |
7.下列各项中表达正确的是( )
| A. | NH3分子的电子式: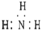 | B. | CH4分子的比例模型: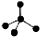 | ||
| C. | O原子的结构示意图: | D. | N2的结构式:N≡N |
10.VmlAl2(SO4)3溶液中,含有Al3+ a g,取$\frac{V}{2}$ml的该溶液稀释到3Vml,则稀释后的溶液中SO42-的物质的量浓度为( )
| A. | $\frac{250a}{27V}$ mol/L | B. | $\frac{250a}{9V}$ mol/L | C. | $\frac{500a}{9V}$ mol/L | D. | $\frac{125a}{9V}$ mol/L |
20. 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关粒子的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关粒子的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关粒子的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关粒子的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )| A. | 当V[NaOH(aq)]=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 | |
| C. | H2A第一步电离的方程式为H2A=HA-+H+ | |
| D. | 向NaHA溶液加入水稀释的过程中,pH可能增大也可能减小 |
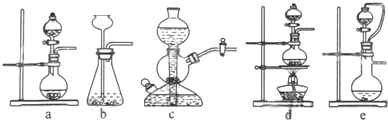
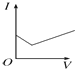

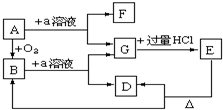 在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白:
在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白: