题目内容
14.某可逆反应从0min~2min进行过程中,在不同反应时间各物质的量的变化情况如图所示.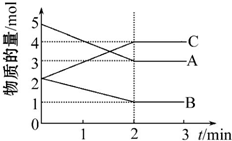
(1)该反应的反应物是A、B,生成物是C.
(2)该反应的化学方程式为2A+B?2C.
(3)反应开始至2min时,能否用C表示反应速率?不能.若能,其反应速率为,若不能,则其原因为不能确定溶液的体积,则不能计算浓度的变化.
(4)2min后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了平衡状态.
分析 (1)从物质的物质的量的变化趋势判断反应物和生成物;
(2)根据物质的物质的量变化值等于化学计量数之比书写化学方程;
(3)化学反应速率是单位时间内浓度的变化,而体积不知;
(4)当反应达到平衡状态时,各物质的物质的量不再变化.
解答 解:(1)由图象可以看出,A、B的物质的量逐渐减小,则A、B为反应物,C的物质的量逐渐增多,作为C为生成物,故答案为:A、B;C;
(2)当反应到达2min时,△n(A)=2mol,△n(B)=1mol,△n(C)=2mol,
化学反应中,各物质的物质的量的变化值与化学计量数呈正比,则△n(A):△n(B):△n(C)=2:1:2,所以反应的化学方程式为:2A+B?2C,故答案为:2A+B?2C;
(3)由于不能确定溶液的体积,则不能计算浓度的变化,无法计算反应速率,故答案为:不能;不能确定溶液的体积,则不能计算浓度的变化;
(4)当反应达到平衡状态时,各物质的物质的量不再变化,2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了平衡状态,故答案为:平衡.
点评 本题考查化学平衡图象问题,题目难度不大,注意把握由图象判断化学方程式的方法.

练习册系列答案
相关题目
5.吸烟者从烟中吸入的主要毒素有CO、致癌物烟焦油,还有( )
| A. | 尼古丁 | B. | CO2 | C. | H2S | D. | NH3 |
2.在恒温、恒容下,当反应容器内总压强不随时间变化时,下列可逆反应一定达到平衡的( )
| A. | 3M(气)+2N(气)?P(气)+4Q(气) | B. | M(气)+2N(气)?3P(气)+Q(固) | ||
| C. | M(气)+N(气)?P(气) | D. | 以上都达到平衡 |
7.下列哪种物质所含的原子数与0.5mol H2O所含原子数相等( )
| A. | 0.6mol H2O2 | B. | 0.5mol H2SO4 | C. | 1mol HNO3 | D. | 1.5mol He |
4.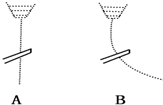 用一带静电的玻璃棒靠近A、B两种纯液体流,现象如图所示据此分析,A、B两种液体分子的极性正确的是( )
用一带静电的玻璃棒靠近A、B两种纯液体流,现象如图所示据此分析,A、B两种液体分子的极性正确的是( )
 用一带静电的玻璃棒靠近A、B两种纯液体流,现象如图所示据此分析,A、B两种液体分子的极性正确的是( )
用一带静电的玻璃棒靠近A、B两种纯液体流,现象如图所示据此分析,A、B两种液体分子的极性正确的是( )| A. | A是极性分子,B是非极性分子 | B. | A是非极性分子,B是极性分子 | ||
| C. | A、B都是极性分子 | D. | A、B都是非极性分子 |
5.下列化合物中,同分异构体数目超过7个的有( )
| A. | 己烷 | B. | 己烯 | C. | 1,2-二溴丙烷 | D. | 乙苯 |
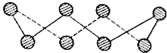 (1)可正确表示原子轨道的是:AC.
(1)可正确表示原子轨道的是:AC.