题目内容
13.可逆反应2NO2$\frac{\underline{\;\;△\;\;}}{\;}$2NO+O2二氧化氮红棕色在密闭容器中反应,达到平衡状态的标志是( )| A. | NO2、NO和O2三者共存 | |
| B. | 单位时间内生成n molO2的同时生成2n mol NO | |
| C. | 容器中颜色不再变化 | |
| D. | 容器中NO2、NO、O2的物质的量浓度之比为2:2:1的状态 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、可逆反应只要反应发生就有反应物和生成物共存的体系,故A错误;
B、单位时间内生成n molO2的同时生成2n mol NO,都反映的是正反应,未体现正与逆的关系,故B错误;
C、容器中颜色不再变化,说明二氧化氮的浓度不变,正逆反应速率相等,故C正确;
D、当体系达平衡状态时,容器中NO2、NO、O2的物质的量浓度之比可能为2:2:1的状态,也可能不是2:2:1,与各物质的初始浓度及转化率有关,故D错误;
故选C.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
3.将X g聚苯乙烯树脂溶于Y L苯中,然后通入Z mol乙炔气体,所得混合液中C、H两元素的质量比为( )
| A. | 6:1 | B. | 12:1 | C. | 1:1 | D. | 1:2 |
4.下列混合物可用加热的方法分离的是( )
| A. | 碘和氯化铵 | B. | 硫酸钾和氯酸钾 | ||
| C. | 氯化铵和硫酸钡 | D. | 碳酸氢钠和碳酸氢铵 |
1.下列属于纯净物的是( )
| A. | 汽油 | B. | 煤 | C. | 乙烯 | D. | 石油裂解气 |
8.下列事实,不能说明氯元素的非金属性比硫元素强的是( )
| A. | 盐酸是强酸,氢硫酸是弱酸 | B. | HClO4酸性比H2SO4强 | ||
| C. | 氯气与H2S能发生置换反应 | D. | 受热时,氯化氢比硫化氢稳定 |
18.下列烃的含氧衍生物中,只能与金属钠反应,不与碳酸氢钠溶液反应的是( )
| A. | CH2=CHCHO | B. | 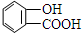 | C. | CH3COOCH3 | D. | 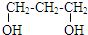 |
5.将铜片和石墨棒用导线相连(其间连有电流表),并同时插入Fe2(SO4)3溶液中,下列现象中不可能出现的是( )
| A. | 铜片质量减少 | B. | 石墨棒质量增加 | C. | 电流表指针偏转 | D. | 溶液显蓝色 |
2.某同学在实验报告中有以下的实验数据:
①用托盘天平称取11.7g食盐
②用量筒量取5.26mL盐酸
③用广泛pH试纸测得溶液的pH是3.5
④用标准NaOH溶液滴定未知浓度的盐酸,用去23.10mL NaOH溶液.
其中数据合理的是( )
①用托盘天平称取11.7g食盐
②用量筒量取5.26mL盐酸
③用广泛pH试纸测得溶液的pH是3.5
④用标准NaOH溶液滴定未知浓度的盐酸,用去23.10mL NaOH溶液.
其中数据合理的是( )
| A. | ①②③ | B. | ①③④ | C. | ①②③④ | D. | ①④ |
3.下列的判断或说法不正确的是( )
| A. | 溶解少量食盐于水中:△S>0 | |
| B. | 自发一定是放热反应 | |
| C. | 自发反应一定是熵增加或者放热反应 | |
| D. | CaCO3 (S) 分解成CaO (S) 和 CO2(g):△S>0 |