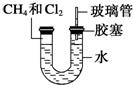
题目内容
12.将甲苯(C7H8)和甘油(C3H8O3)以一定比例混合,测得混合物含碳51.3%,则氧的质量分数为( )| A. | 40% | B. | 35% | C. | 30% | D. | 无法计算 |
分析 甲苯、甘油的相对分子质量均为92,两种有机物ω(H)相同,则可计算含氧量.
解答 解:甲苯、甘油的相对分子质量均为92,由于两种有机物的H原子数目相等,则ω(H)为定值,故ω(H)=$\frac{8}{92}$=8.7%,又含碳51.3%,则氧元素的质量分数是1-51.3%-8.7%=40%,故选A.
点评 本题考查质量分数的计算,题目难度不大,本题注意比较分子式的组成计算含氢量为解答该题的关键.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
3.下列分子中,所有原子的最外层均为8电子结构的是( )
| A. | BeCl2和PCl5 | B. | HClO和SO2 | C. | P4和COS(羰基硫) | D. | SiO2和NaCl |
20.在一个1L的容器中,加入2molA和1molB,发生下述反应:2A(g)+B(g)?3C(g)+D(s).平衡时,C的浓度为1.2mol/L.维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,下列组合能达到的是( )
| A. | 6molC+xmolD(x>0.6) | |
| B. | 1molA+0.5molB+1.5molC+xmolD(x>0.1) | |
| C. | 3molA+1.5molB+x molD(x≥0) | |
| D. | 1molA+0.5molB+3molC+xmolD(x>0) |
7.结合如图判断,下列叙述正确的是( )
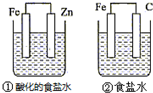

| A. | ①和②中铁的腐蚀均被加速 | |
| B. | ①和②中负极反应均是Fe-2e-═Fe2+ | |
| C. | ②中碳棒上反应是O2+2H2O+4e-═4OH- | |
| D. | ①装置中溶液pH会升高,②装置中溶液碱性增强 |
17.某化学反应过程如图所示,由图得出的判断,正确的是( )
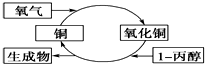

| A. | 生成物是丙酮 | |
| B. | 1-丙醇发生了还原反应 | |
| C. | 反应中有红黑颜色交替变化的现象发生 | |
| D. | 醇类都能发生图示的催化氧化反应 |
1.下列说法正确的是( )
| A. | NH4Cl溶液加水稀释,恢复至室温后,pH变大 | |
| B. | 稀释0.1 mol•L-1醋酸溶液,溶液中离子的浓度均变小 | |
| C. | 在 NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 将A1C13溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体的成分相同 |
2. 一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意图如图.下面对这种电池的说法不正确的是( )
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意图如图.下面对这种电池的说法不正确的是( )
 一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意图如图.下面对这种电池的说法不正确的是( )
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2═2CO2+3H2O,电池示意图如图.下面对这种电池的说法不正确的是( )| A. | 该电池在工作时,溶液中的阳离子向正极移动 | |
| B. | 设每个电子所带电量为q库仑,NA表示阿伏加德罗常数,则46g乙醇被氧化产生12NAq库仑的电量 | |
| C. | 电池工作时电子由a极沿导线经灯泡再到b极 | |
| D. | 电池正极的电极反应式为:O2+4e-+2H2O═4OH- |