题目内容
3.下列分子中,所有原子的最外层均为8电子结构的是( )| A. | BeCl2和PCl5 | B. | HClO和SO2 | C. | P4和COS(羰基硫) | D. | SiO2和NaCl |
分析 原子的最外层电子数+化合价绝对值=8,则该原子的最外层为8电子结构,以此来解答.
解答 解:A.Be原子最外层为4电子结构,P原子最外层为10电子结构,故A不选;
B.H原子最外层为2电子结构,S原子最外层为6电子结构,故B不选;
C.白磷为 正四面体结构,P最外层电子为5+3=8,COS的结构式为S=C=O,则均满足最外层8电子,故C选;
D.SiO2为原子晶体,不存在分子,且NaCl为离子化合物,不存在分子,故D不选;
故选C.
点评 本题考查分子的结构及化学键,为高频考点,把握判断最外层电子判断的规律及最外层电子数为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
18.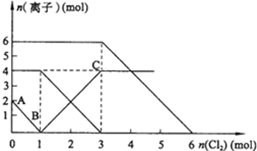 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )
 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )| A. | BC段为Fe3+的变化曲线 | |
| B. | 原混合溶液中FeBr2的物质的量为6mol | |
| C. | 当通入2mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
15.类推是在化学学习和研究中常用的思维方法,但类推出的结论最终要经过实践的检验才能决定其正确与否,下列几种类推结论中错误的是( )
| A. | 由Fe跟S直接化合可得FeS,类推出Cu跟S直接化合可得Cu2S | |
| B. | 金属镁失火不能用CO2灭火,金属钠失火也不能用CO2灭火 | |
| C. | NH4Cl、NH4I结构相似,将两种固体分别加热,分解都只生成卤化氢和氨气 | |
| D. | 原电池中通常是活泼金属做负极,不活泼金属做正极,用镁和铝与NaOH溶液构成原电池时,镁是负极 |
12.将甲苯(C7H8)和甘油(C3H8O3)以一定比例混合,测得混合物含碳51.3%,则氧的质量分数为( )
| A. | 40% | B. | 35% | C. | 30% | D. | 无法计算 |
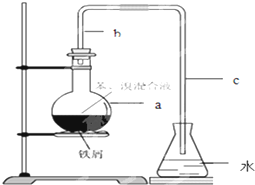 化学课外小组用如图装置制取溴苯.
化学课外小组用如图装置制取溴苯. .
.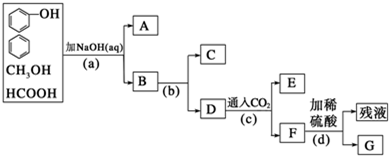
 某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:
某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目: