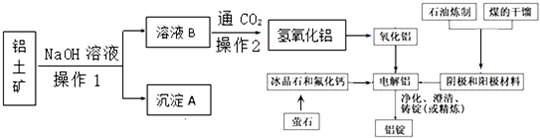
题目内容
17. A,B,C,D,E是五种短周期元素,A,B,C,D,E分别代表元素符号,他们的原子序数依次增大,A是元素周期表中半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐;D与A同主族,且与E同周期;E元素最外层电子数是其次外层电子数的$\frac{3}{4}$;C与E同主族.请回答下列问题:
A,B,C,D,E是五种短周期元素,A,B,C,D,E分别代表元素符号,他们的原子序数依次增大,A是元素周期表中半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐;D与A同主族,且与E同周期;E元素最外层电子数是其次外层电子数的$\frac{3}{4}$;C与E同主族.请回答下列问题:(1)D元素在元素周期表中的位置是第三周期IA族;
(2)元素的非金属性C>E(填“>”或“<”),下列各项中,能说明这一结论的事实是②③(填序号).
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
(3)已知:NaOH溶液与BC气体不反应;NaOH溶液与BC2反应的化学方程式为:2BC2+2NaOH═NaBC2+BaBC3+H2O;NaOH与BC2,BC的混合气体反应的化学方程式为:BC2+BC+2NaOH═2NaBC2+H2O,若BC2和BC组成的混合气体通入氢氧化钠溶液后,气体被完全吸收,无剩余.则n(BC2)与n(BC)的关系为n(NO2)≥n(NO).
(4)在容积为1.00L的容器中,通入一定量的B2C4,发生反应B2C4(g)?2BC2(g),100℃时,体系中各物质浓度随时间变化如图所示.回答下列问题:
①若温度升高,混合气体的颜色变深,则该反应的△H>0(选填“>”或“<”).
②100℃时该反应的平衡常数K为0.36.
分析 短周期元素A、B、C、D、E的原子序数依次增大,A元素的原子是半径最小的原子,则A为H元素;B元素的最高价氧化物的水化物与其氢化物反应生成一种盐,则B为N元素;D与A同主族,D的原子序数大于N,则D为Na;D且与E同周期,则E为第三周期元素,其次外层电子数为8,最外层电子数为$\frac{3}{4}$×8=6,则E为S元素;C与E同主族,则C为O元素,据此解答.
解答 解:短周期元素A、B、C、D、E的原子序数依次增大,A元素的原子是半径最小的原子,则A为H元素;B元素的最高价氧化物的水化物与其氢化物反应生成一种盐,则B为N元素;D与A同主族,D的原子序数大于N,则D为Na;D且与E同周期,则E为第三周期元素,其次外层电子数为8,最外层电子数为$\frac{3}{4}$×8=6,则E为S元素;C与E同主族,则C为O元素.
(1)D为Na元素,在元素周期表中的位置是:第三周期IA族,故答案为:第三周期IA族;
(2)同主族自上而下非金属性减弱,故元素的非金属性C(氧)>E(硫),
①氢化物酸性强弱不能比较元素非金属性强弱,故错误;
②元素非金属性与氢化物稳定性一致,非金属性越强,大于氢化物越稳定,故正确;
③H2S的水溶液放置在空气中会变浑浊,说明氧气置换出硫单质,则氧元素非金属性较强,故正确,
故答案为:>;②③;
(3)NaOH溶液与NO气体不反应;NaOH溶液与NO2反应的化学方程式为:2NO2+2NaOH═NaNO2+BaNO3+H2O;NaOH与NO2、NO的混合气体反应的化学方程式为:NO2+NO+2NaOH═2NaNO2+H2O,若NO2和NO组成的混合气体通入氢氧化钠溶液后,气体被完全吸收,无剩余,由方程式可知n(NO2)≥n(NO),
故答案为:n(NO2)≥n(NO);
(4)在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),
①若温度升高,混合气体的颜色变深,说明升高温度平衡正向移动,则该反应的△H>0,故答案为:>;
②100℃时,平衡时N2O4的浓度为0.04mol/L,NO2浓度为0.12mol/L,则100℃时该反应的平衡常数K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$=$\frac{0.1{2}^{2}}{0.04}$=0.36,故答案为:0.36.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意金属性、非金属性强弱比较实验事实.

 某温度时,在2L密闭容器中有X、Y、Z三种气态物质,实验测得不同时刻各物质的量如下表所示,同时测得至3min时吸收热量75kJ.
某温度时,在2L密闭容器中有X、Y、Z三种气态物质,实验测得不同时刻各物质的量如下表所示,同时测得至3min时吸收热量75kJ. | t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.60 | 0.20 | 0.80 |
| 14 | 0.60 | 0.20 | 0.80 |
(2)该温度下反应的平衡常数K=$\frac{1600}{9}$.
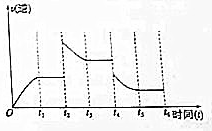
(3)若该反应的逆反应速率与时间的关系如图所示.则:
①t2~t3时平衡向逆(填“正”或“逆”)反应方向移动.
②t4时被改变的外界条件是B(选择一个正确选项)
A升温 B降温 C.降压 D.移去部分反应物 E加入负催化剂.
| A. | 再通入少量氯气,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小 | |
| B. | 光照一段时间氯水,溶液的pH值增大 | |
| C. | 加入少量固体AgNO3,溶液的pH值减小 | |
| D. | 加入少量水,水的电离平衡向右移动 |
C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H1=-a kJ•mol-1 ①
C3H8(g)+5O2(g)═3CO2(g)+4H2O(g)△H2=-b kJ•mol-1 ②
下列判断正确的是( )
| A. | △H1>△H2 | B. | a=b | C. | a>b | D. | a<b |
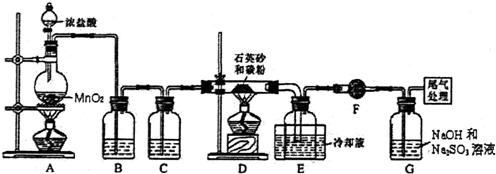
已知SiCl4的熔点为-70.0℃,沸点为57.7℃,且遇水易反应,
请回答下列问题:
(1)写出装置A中发生反应的离子方程式:MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑
(2)装置B中的试剂是饱和食盐水;装置C的作用为干燥氯气
(3)装置D的玻璃管中发生主要反应的化学方程式是SiO2+2C+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SiCl4+2CO,装置F的作用为防止F右端的水蒸气进入E与四氯化硅反应,造成产物不纯.
(4)G中吸收气体一段时间后,吸收液中肯定存在OH-、Cl-和SO42-.为探究该吸收液中可能存在的其它酸根离子(忽略空气中CO2的影响),研究小组实验设计如下
【提出假设】假设1:只有SO32-:假设2:既无SO32-也无ClO-;假设3:只有ClO-:
【设计方案,进行试验】可供选择的实验试剂有:3mol/L H2SO4溶液、1mol/L NaOH溶液、品红溶液、0.01mol/L KMnO4溶液、淀粉-KI溶液.各取少量吸收液于a、b、c三支试管中,分别滴加3mol/L H2SO4酸化后,进行下列实验:
请完成如表:
| 序号 | 操作 | 可能出现的现象 | 结论 |
| ① | 向a试管中滴加几滴0.01mol/L的KMnO4 | 若溶液褪色 | 则假设1成立 |
| 若溶液不褪色 | 则假设2或3成立 | ||
| ② | 向b试管中滴加几滴品红 | 若溶液褪色 | 则假设1或3成立 |
| 若溶液不褪色 | 则假设2成立 | ||
| ③ | 向c试管中滴加几滴淀粉-KI溶液 | 则假设3成立 |