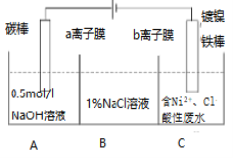
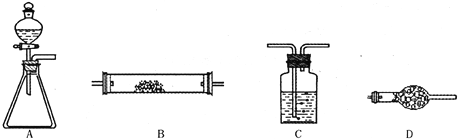
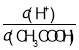题目内容
【题目】某校学生实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,气密性已检验,F是用于鼓入空气的双连打气球)。
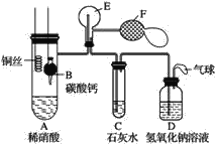
实验操作及现象为:
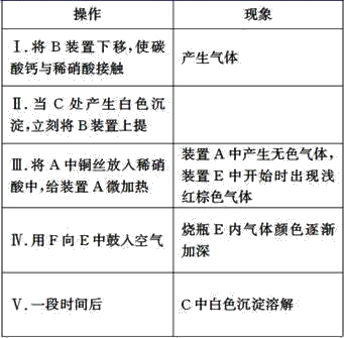
(1)操作Ⅰ中产生气体的离子反应方程式为__;
(2)操作Ⅰ的目的是__;
(3)C中白色沉淀的化学式是__,操作Ⅱ中当C产生白色沉淀时立刻将B上提的原因是__;
(4)操作Ⅲ中装置A产生无色气体的化学方程式是__;
(5)烧瓶E内气体颜色逐渐加深的原因是__;
(6)操作Ⅴ现象产生的原因是(结合化学方程式说明)__;
(7)D装置的作用是__。
【答案】CaCO3+2HNO3=Ca(NO3)2+H2O+CO2↑ 用碳酸钙与稀硝酸反应产生的二氧化碳气体赶走装置内的空气 CaCO3 防止消耗硝酸过多影响铜与硝酸的反应 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O CO2比空气密度大,从长管进入E,没有把E中空气赶净,使部分NO先与空气生成少量红棕色二氧化氮气体,当再从F鼓入空气时,E中又生成二氧化氮气体,红棕色加深 C中白色沉淀溶解是因为氮氧化物和空气一起通过溶液会生成硝酸,4NO+3O2+2H2O=4HNO3,4NO2+O2+2H2O=4HNO3,硝酸能溶解碳酸钙沉淀 平衡压强,吸收氮氧化物、二氧化碳等尾气,防止污染空气
【解析】
该实验的原理是首先用碳酸钙与稀硝酸反应产生的CO2将装置中的空气排尽,以防止空气中的氧气对实验造成干扰,然后铜与稀硝酸反应产生气体,通过向E装置中通入空气,气体颜色变深,说明铜与稀硝酸反应产生的气体为NO,最后处理尾气。
(1)碳酸钙和硝酸反应生成二氧化碳赶净装置中的空气;
(2)操作Ⅰ的目的是用碳酸钙与稀硝酸反应产生的二氧化碳气体赶走装置内的空气;
(3)C中出现白色沉淀说明E中空气赶净,生成的沉淀为碳酸钙,C中白色沉淀的化学式是CaCO3,将B上提的原因是减少硝酸消耗量;
(4)铜和稀硝酸加热反应生成硝酸铜,一氧化氮和水,该化学方程式为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
(5)二氧化碳比空气密度大,未赶净E中的空气,生成的一氧化氮气体遇到空气中的氧气会生成二氧化氮红棕色气体,F鼓入空气更多的一氧化氮和氧气反应生成二氧化氮气体;
(6)操作Ⅴ现象产生的原因是,C中白色沉淀溶解是因为氮氧化物和空气一起通过溶液会生成硝酸,4NO+3O2+2H2O=4HNO3,4NO2+O2+2H2O=4HNO3,硝酸能溶解碳酸钙沉淀。
(7)D装置中的气球可以平衡压强,吸收氮氧化物、二氧化碳,防止污染空气。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案