题目内容
8.下列实验方案合理的是( )| A. | 制备乙炔:实验室不能用启普发生器来制取乙炔 | |
| B. | 制备乙酸乙酯:将乙醇和乙酸混合,再加入稀硫酸共热 | |
| C. | 制备一氯乙烷:将乙烷和氯气的混合气放在光照条件下反应 | |
| D. | 制备乙烯:实验室用无水乙醇和浓硫酸共热到170℃制取乙烯 |
分析 A.生成氢氧化钙微溶,易堵塞启普发生器瓶颈;
B.需要浓硫酸作催化剂和吸水剂;
C.光照下的取代反应为链锁反应;
D.无水乙醇和浓硫酸共热到170℃,发生消去反应.
解答 解:A.生成氢氧化钙微溶,易堵塞启普发生器瓶颈,则实验室不能用启普发生器来制取乙炔,可利用制取氢气的简易装置制备乙炔,故A正确;
B.制备乙酸乙酯,需要浓硫酸作催化剂和吸水剂,先加乙醇,再加浓硫酸,最后加乙酸,故B错误;
C.光照下的取代反应为链锁反应,则制备一氯乙烷不能利用光照下取代反应,应选乙烯和HCl反应制取,故C错误;
D.无水乙醇和浓硫酸共热到170℃,发生消去反应,可制取乙烯,故D正确;
故选AD.
点评 本题考查化学实验方案的评价,为高频考点,涉及有机物的性质及制备,把握性质及反应原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.已知标准状况下11.2LA气体分子的质量为16g,则A气体的摩尔质量是( )
| A. | 16g | B. | 32g | C. | 64g/mol | D. | 32g/mol |
16.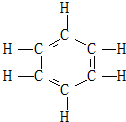 1866年凯库勒提出了苯的单、双键交替的正六边形平面结构(如图),解释了苯的部分性质,但还有一些问题尚未解决,如它不能解释( )
1866年凯库勒提出了苯的单、双键交替的正六边形平面结构(如图),解释了苯的部分性质,但还有一些问题尚未解决,如它不能解释( )
①苯不能使溴的CCl4溶液褪色;②苯能与H2发生加成反应
③溴苯没有同分异构体 ④邻二溴苯只有一种.
 1866年凯库勒提出了苯的单、双键交替的正六边形平面结构(如图),解释了苯的部分性质,但还有一些问题尚未解决,如它不能解释( )
1866年凯库勒提出了苯的单、双键交替的正六边形平面结构(如图),解释了苯的部分性质,但还有一些问题尚未解决,如它不能解释( )①苯不能使溴的CCl4溶液褪色;②苯能与H2发生加成反应
③溴苯没有同分异构体 ④邻二溴苯只有一种.
| A. | ①④ | B. | ④ | C. | ②③ | D. | ② |
13.下列离子方程式书写正确的是( )
| A. | 硅酸钠溶液中逐滴加入盐酸:Na2SiO3+2H+=H2SiO3↓+2Na2+ | |
| B. | 向氢氧化钠溶液中加入醋酸溶液:OH-+H+=H2O | |
| C. | 铜与稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| D. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
20.德国人弗里茨•哈伯(Fritz Haber)由于发明了合成氨的方法而获得了1918年诺贝尔化学奖,他的发明大大提高了农作物的产量,同时也提高了硝酸、炸药的产量.下列有关说法正确的是( )
| A. | N2和H2在点燃或光照条件下合成氨 | |
| B. | 氨的稳定性比磷化氢弱 | |
| C. | 氨极易溶于水,氨水呈碱性,主要含 NH4+和OH- | |
| D. | 由氨制取硝酸铵的过程中,氨表现出还原性和碱性 |
17.设NA为阿佛加德罗常数,下列说法不正确的是(相对原子质量 Na:23 O:16 H:1)( )
| A. | 78gNa2O2固体中含有的阴离子数为2NA | |
| B. | 18g水中含有的电子数为10NA | |
| C. | 常温常压下,金属钠从水中置换出22.4LH2,发生转移的电子数小于2NA | |
| D. | 在1L2mol/L的硝酸铝溶液中含有的铝离子数为2NA |
18.下列说法正确的是( )
| A. | 离子化合物中一定含有金属阳离子 | |
| B. | 离子化合物中只含有离子键 | |
| C. | 在酸碱盐中,碱与盐一定属于离子化合物 | |
| D. | 离子键一定存在于化合物中 |
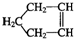 可简写为
可简写为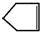 .降冰片烯的分子结构可表示为:
.降冰片烯的分子结构可表示为: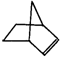
 .
.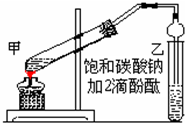 实验室制取乙酸乙酯的主要步骤如下:
实验室制取乙酸乙酯的主要步骤如下: