题目内容
7.莽草酸可用于合成药物达菲,其结构简式(如图),下列关于莽草酸的说法正确的是( )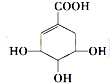
| A. | 分子式为C7H6O5 | |
| B. | 分子中含有的官能团有羟基、酯基、碳碳双键 | |
| C. | 可发生加成反应、取代反应、氧化反应、还原反应 | |
| D. | 在水溶液中羧基和羟基均能电离出H+,1mol达菲可与4mol Na反应生成2 mol H2 |
分析 该分子中含有碳碳双键、醇羟基和羧基,具有烯烃、醇、羧酸的性质,能发生加成反应、氧化反应、酯化反应、消去反应、还原反应等,据此分析解答.
解答 解:A.根据结构简式知,分子式为C7H10O5,故A错误;
B.含有的官能团有羟基、羧基和碳碳双键,故B错误;
C.该分子中含有碳碳双键、醇羟基和羧基,具有烯烃、醇、羧酸的性质,能发生加成反应、氧化反应、酯化反应、消去反应、还原反应等,故C正确;
D.含有羧基和醇羟基,羧基能电离出氢离子,醇羟基和羧基能和钠反应生成氢气,故D错误;
故选C.
点评 本题考查有机物结构和性质,明确官能团及其性质关系即可解答,侧重考查羧酸、醇、烯烃的性质,题目难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
17.人们在远距离运输果实或花朵时,装有果实或花朵的密闭容器中,常常放有浸泡过KMnO4(aq)的硅土,其作用是( )
| A. | 给容器消毒 | B. | 杀死果实周围的细菌,防止霉变 | ||
| C. | 延长果实或花朵的寿命 | D. | 催熟果实或花朵 |
15.现有几组物质的熔点(℃)数据:
据此回答下列问题:
(1)A组属于原子晶体,其熔化时克服的粒子间的作用力是化学键.
(2)B组晶体共同的物理性质是②③④(填序号).
①硬度大 ②导电性 ③导热性 ④延展性
(3)D组晶体可能具有的性质是②④(填序号).
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(4)D组晶体的熔点由高到低的顺序为:NaCl>KCl>RbCl>CsCl,其原因解释为:都为离子晶体,r(Na+)<r(K+)<r(Rb+)<r(Cs+),在离子所带电荷相同的情况下,半径越小,晶格能越大,熔点就越高.
| A组 | B组 | C组 | D组 |
| 金刚石:3550 | Li:181 | HF:-83 | NaCl:801 |
| 硅晶体:1410 | Na:98 | HCl:-115 | KCl:776 |
| 硼晶体:2300 | K:64 | HBr:-89 | RbCl:718 |
| 二氧化硅:1710 | Rb:39 | HI:-51 | CsCl:645 |
(1)A组属于原子晶体,其熔化时克服的粒子间的作用力是化学键.
(2)B组晶体共同的物理性质是②③④(填序号).
①硬度大 ②导电性 ③导热性 ④延展性
(3)D组晶体可能具有的性质是②④(填序号).
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(4)D组晶体的熔点由高到低的顺序为:NaCl>KCl>RbCl>CsCl,其原因解释为:都为离子晶体,r(Na+)<r(K+)<r(Rb+)<r(Cs+),在离子所带电荷相同的情况下,半径越小,晶格能越大,熔点就越高.
12.(1)①下表为烯烃类化合物与溴发生加成反应的相对速率(以乙烯为标准).
据表中数据,总结烯烃类化合物加溴时,反应速率与C=C上取代基的种类、个数间的关系:C=C上取代基为烃基的反应速率快,烃基越多反应速率越快,C=C上取代基为卤素原子的反应速率慢,卤素原子越多反应速率越慢.
②下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是D.
A.(CH3)2C=C(CH3) 2 B.CH3CH=CHCH3C.CH2CH=CH2 D.CH2=CHCl
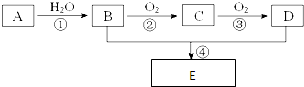
(2)已知A是化工生产中重要的气态烃,在标准状况下的密度为1.25g/L,现以A为主要原料合成E,其合成路线如图所示.回答下列问题:①写出A的电子式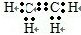 .
.
②写出下列反应的化学方程式:
第①步CH2=CH2+H2O→CH3CH2OH;
第③步2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH;
③已知A在有催化剂条件下可以与氧气反应直接制得C,写出该反应的化学方程式2CH2=CH2+O2$\stackrel{催化剂}{→}$2CH3CHO
| 烯烃类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
②下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是D.
A.(CH3)2C=C(CH3) 2 B.CH3CH=CHCH3C.CH2CH=CH2 D.CH2=CHCl
(2)已知A是化工生产中重要的气态烃,在标准状况下的密度为1.25g/L,现以A为主要原料合成E,其合成路线如图所示.回答下列问题:①写出A的电子式
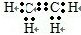 .
.②写出下列反应的化学方程式:
第①步CH2=CH2+H2O→CH3CH2OH;
第③步2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH;
③已知A在有催化剂条件下可以与氧气反应直接制得C,写出该反应的化学方程式2CH2=CH2+O2$\stackrel{催化剂}{→}$2CH3CHO

19.下列关于有机物的说法正确的是( )
| A. | 煤的液化是物理变化 | |
| B. | 石油干馏可得到汽油、煤油等 | |
| C. | 淀粉、蛋白质完全水解的产物互为同分异构体 | |
| D. | 乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
16.能够鉴定氯乙烷中氯元素的存在的操作是( )
| A. | 在氯乙烷中直接加入AgNO3溶液 | |
| B. | 加蒸馏水,然后加入AgNO3溶液 | |
| C. | 加入NaOH溶液,加热后酸化,然后加入AgNO3溶液 | |
| D. | 加入NaOH的乙醇溶液,然后加入AgNO3溶液 |
18.下列事实不能作为实验判断依据的是( )
| A. | 钠和镁分别与冷水反应,判断金属活动性强弱 | |
| B. | 铁投入CuSO4溶液中,能置换出铜,钠投入CuSO4溶液中不能置换出铜,判断钠与铁的金属活动性强弱 | |
| C. | 酸性H2CO3<H2SO4,判断硫与碳的非金属活动性强弱 | |
| D. | Br2与I2分别与足量的H2反应,判断溴与碘的非金属活动性强弱 |
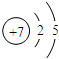 .
.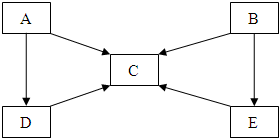 A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D、E在常温下都是气体,B为红棕色.
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D、E在常温下都是气体,B为红棕色.