题目内容
8.将一定量氢气通过0.1mol灼热的氧化铜,反应一段时间冷却后称量剩余固体质量为7.2g,则参加反应的CuO为( )| A. | 0.4g | B. | 0.1mol | C. | 0.05mol | D. | 8g |
分析 氢气和氧化铜反应生成了铜和水,分析反应的特点可以知道,反应前后固体质量差为氧化铜在反应中失去氧元素的质量,失去的氧元素与氢化合成水,因此,由氧元素质量可计算生成水的质量,消耗掉的氧化铜的质量,可以据此完成该题的解答.
解答 解:分析反应的特点可以知道,反应前后固体质量差为氧化铜在反应中失去氧元素的质量,0.1mol灼热的氧化铜质量是8g,其质量为8g-7.2g=0.8g:
设生成水的质量为x,生成铜的质量为y,参加反应的氧化铜的质量为z,
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O 固体质量减少
80 64 18 16
z y x 0.8g
$\frac{18}{x}$=$\frac{64}{y}$=$\frac{80}{z}$=$\frac{16}{0.8}$,解得:z=4g,所以参加反应的CuO为4g,物质的量是$\frac{4g}{80g/mol}$=0.05mol,故选C.
点评 根据化学方程式进行计算时,所使用的物质的质量必须为完全反应时物质的质量,未参加反应的物质的质量不能代入化学方程式进行计算.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
19.化学与科学、技术、社会、环境密切相关.下列有关说法不正确的是( )
| A. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| B. | 高纯度的二氧化硅广泛用于制作光导纤维,遇强碱会“断路” | |
| C. | 以NO和N02为主的氮氧化物是形成光化学烟雾和酸雨的一个重要原因 | |
| D. | FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
16.下列叙述中,指定粒子的数目约为6.02×1023的是( )
| A. | 11.2 L Cl2中含有的氯原子数 | |
| B. | 常温常压下,1.6 g CH4中含有的质子数 | |
| C. | 标准状况下,22.4 L H2O中含有的氧原子数 | |
| D. | 1 mol Na2SO4溶于水,所得溶液中含有的钠离子数 |
3.下列说法不正确的是( )
| A. | 天然气的主要成分是甲烷 | |
| B. | 煤是由有机物和无机物组成的复杂的混合物 | |
| C. | 含C18以上烷烃的重油经裂化可以得到汽油 | |
| D. | 煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 |
20.下列化学用语正确的是( )
| A. | 乙烯分子的最简式:CH2 | B. | 己烷的分子式:C6H12 | ||
| C. | 羟基的化学式:OH- | D. | 1,2-二溴乙烷的结构简式:C2H4Br2 |
17.下列说法正确的是( )
| A. | 甲醛、氯乙烯和乙二醇均可作为合成聚合物的单体 | |
| B. | 麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原性二糖 | |
| C. | 若两种二肽互为同分异构体,则二者的水解产物一定不同 | |
| D. | 天然植物油常温下一般呈液态,难溶于水,有恒定的熔点、沸点 |
18.下列反应既是氧化还原反应又是吸热反应的是( )
| A. | Ba(OH)2•8H2O与NH4Cl反应 | |
| B. | 葡萄糖在人体内氧化分解 | |
| C. | 二氧化碳与赤热的碳反应生成一氧化碳 | |
| D. | 锌粒与稀H2SO4反应制取H2 |
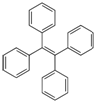 四苯基乙烯是一种在建筑及医疗设备、包装和电器制造中使用的化合物,结构如图.它的一氯代物有3种,分子中能共面的碳原子最多有26个.
四苯基乙烯是一种在建筑及医疗设备、包装和电器制造中使用的化合物,结构如图.它的一氯代物有3种,分子中能共面的碳原子最多有26个.