��Ŀ����
����Ŀ�����ճ������У�Ϊ�˴ﵽ���õ����Ч�����������˻Ὣ���Һ(��������)��84����Һ���ʹ�ã��Ӷ��ᷢ�������ж����¹ʡ�
��1�������ջ���Ʒ��Ҫ�ɷ��ж�������Ԫ�أ���Ԫ����Ԫ�����ڱ���λ���� ��
��2��84����Һ����Ҫ�ɷ��Ǵ������ƣ�д���������Ƶĵ���ʽ�� ��
��3�������£�0��1mol/L��NaClO��Һ��PH=9��7��ԭ�� ��������HClO�ĵ���ƽ�ⳣ��Ϊ �����Һ��84����Һ��Ϻ�������ж���������д���÷�Ӧ�����ӷ���ʽ ��
��4�����������һ�ָ�Ч���ˮ����������ҵ�ϳ�����NaClO��������������Ӧԭ��Ϊ��
���ڼ��������£�����NaClO�������������Ƶ�Na2FeO4���÷�Ӧ�����ӷ�Ӧ����ʽΪ ��
��Na2FeO4��KOH��Ӧ����K2FeO4��Na2FeO4+2KOH=K2FeO4+2NaOH��K2FeO4��ˮ��Һ����ˮ�⣺4FeO42-+10H2O![]() 4Fe(OH)3+8OH-+3O2�������ᴿ��K2FeO4�в����ؽᾧ��ϴ�ӡ����º�ɵķ�������ϴ�Ӽ����ѡ�� ��Һ(�����)
4Fe(OH)3+8OH-+3O2�������ᴿ��K2FeO4�в����ؽᾧ��ϴ�ӡ����º�ɵķ�������ϴ�Ӽ����ѡ�� ��Һ(�����)
a��ˮ b��NH4Cl������� c��Fe(NO3)3������� d��CH3COONa�������
���𰸡�
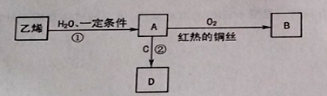
��1����3������A�� ��
��2��![]()
��3��ClO-+H2O ![]() HClO+OH- ��10-6.4 �� ClO-+ Cl-+2H+ =Cl2+H2O
HClO+OH- ��10-6.4 �� ClO-+ Cl-+2H+ =Cl2+H2O
��4����2Fe3++3ClO- +10OH- =2FeO42- +5H2O +3Cl- ����d
��������
�����������1���ȵ�ԭ������Ϊ17��ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ7����Ӧλ�����ڱ�����������A�壬�ʴ�Ϊ������������A �壻
(2 )�������������ӻ������ԭ�Ӻ���ԭ�ӹ���1�Թ��õ��Ӷԣ�����ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��3�������£�0.1mol/L��NaClO��Һ��pH=9.7����Һ�Լ��ԣ�����������Һ�д����������ˮ���Լ��ԣ���Ӧ�����ӷ���ʽΪ��ClO-+H2O![]() HClO+OH-�������£�0.1mol/L��NaClO��Һ��pH=9.7��ClO-+H2O
HClO+OH-�������£�0.1mol/L��NaClO��Һ��pH=9.7��ClO-+H2O![]() HClO+OH-��Kh=
HClO+OH-��Kh=![]() =
=![]() ����Ka=
����Ka=![]() �T10-6.4������������ǿ�����ԣ�������ǿ��ԭ�ԣ�������������������ԭ��Ӧ��������������ʽΪ��NaClO+2HCl�TNaCl+Cl2��+H2O�����ӷ���ʽΪ��ClO-+Cl-+2H+=Cl2��+H2O���ʴ�Ϊ�������������ˮ����Һ�Լ��ԣ�ClO-+H2O
�T10-6.4������������ǿ�����ԣ�������ǿ��ԭ�ԣ�������������������ԭ��Ӧ��������������ʽΪ��NaClO+2HCl�TNaCl+Cl2��+H2O�����ӷ���ʽΪ��ClO-+Cl-+2H+=Cl2��+H2O���ʴ�Ϊ�������������ˮ����Һ�Լ��ԣ�ClO-+H2O![]() HClO+OH-��10-6.4��ClO-+Cl-+2H+=Cl2��+H2O��
HClO+OH-��10-6.4��ClO-+Cl-+2H+=Cl2��+H2O��
��4�����ڼ��������£�����NaClO�������������Ƶ�Na2FeO4���÷�Ӧ�����ӷ�Ӧ����ʽΪ2Fe3++3ClO-+10OH-=2FeO42-+5H2O+3Cl-���ʴ�Ϊ��2Fe3++3ClO-+10OH-=2FeO42-+5H2O+3Cl-����Ϊ����K2FeO4��ˮ�⣬Ӧ�ڼ���������ϴ�ӣ�����CH3COONa��Ϊ��ֹK2FeO4���ܽ⣬���������ϴ�ӣ��ʴ�Ϊ��d��

����Ŀ���̵ĵ��ʼ��仯�������������������й㷺Ӧ�á�
��1������п�̵�ع㷺Ӧ�����ճ������ص��ܷ�ӦʽΪ��Zn(s)��2MnO2(s)��2H2O(l)===Zn(OH)2(s)��2MnOOH(s)���õ�ص�������ӦʽΪ ��
��2��ijѧϰС�����ԷϾɸɵ��Ϊԭ����ȡ�̣������������£�
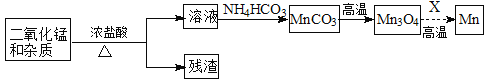
������Ũ�����ܽ�Ͼɵ���ں�ɫ���ʹ����б���ͨ�磬��ԭ���� ��
���Ӳ�Ʒ���ȡ������ȽǶȿ��ǣ�X��ѡ�� ������ţ���
A����̿ B���� C������ D��һ����̼
��д��̼�����ڿ����������������������̵Ļ�ѧ����ʽ ��
��3�������������Һ�������ֽ�ʪ��ұ�̡������̿���Ҫ�ɷ���MnCO3����Ҫ������Fe2+��Co2+��Ni2+��Ϊԭ���Ʊ��̵Ĺ����������£�
![]()
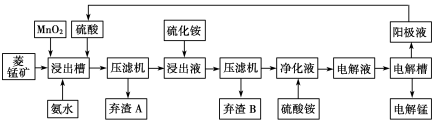
��֪��NiS ��CoS��������ˮ���������������pH���±�������ij����Ũ��С�ڵ���105mol��L1������Ϊ��ȫ������
���� | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 | Fe(OH)3 |
��ʼ����pH | 7.5 | 7.7 | 7.6 | 8.3 | 2.7 |
��ȫ����pH | 9.7 | 8.4 | 8.5 | 9.8 | 3.8 |
����������MnO2�������ǣ������ӷ���ʽ��ʾ�� ��
�����백ˮ���ڽ���������Һ��pH��ΧΪ ��
�����������ĵ缫��ӦʽΪ ��