��Ŀ����
����Ŀ��25�桢101kPa�£�ϡǿ����ϡǿ����Һ��Ӧ�к���Ϊ57.3kJ/mol��
��1��д����ʾϡH2SO4��ϡ�ռ���Һ��Ӧ���к��ȵ��Ȼ�ѧ����ʽ��___��
��2��ѧ������50mL0.25mol/L������50mL0.55mol/L�ռ���Һ�ⶨ�к���װ����ͼ��
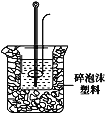
��ʵ��ʱ����IJ����������ձ�����Ͳ��裺__��
�ڸ�װ������һ�������ǣ�___������øô���װ�òⶨ����õ��к�����H��___(����ƫ��ƫС����Ӱ����)��
�������60mL0.25mol/L������50mL0.55mol/LNaOH��Һ���з�Ӧ��������ʵ����ȣ������к���___(������ȡ��������)��
������Ӧǰ��Һ�Լ��кͺ�Ļ��Һ���ܶȾ���Ϊ1g/cm3�����ǰ�������¶Ⱦ�Ϊt1����Ϻ���Һ���¶�Ϊt2��������Ϊ4.18J/(g����)�����к�����H=___��
��3��ѧ������2mol/L���������ⶨ��п����п�۷�Ӧ�Ŀ����������ͼװ�ã�
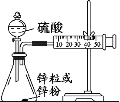
��������ʵ��ⶨʱ����趨Ϊ10min��������Ҫ�ⶨ����һ�������ǣ�___��
����Ҫ��С����H2�����ʶ��ֲ�Ӱ�����H2��������Ӧ�������м���___(����ĸ)
a.Na2CO3��Һ b.K2SO4��Һ c.NaNO3��Һ d.ˮ e.CuSO4��Һ
���𰸡�NaOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)+H2O(l) ��H=-57.3kJ/mol �¶ȼƺͻ��β�������� ���ձ���û�и�Ӳֽ�����ĭ���ϰ� ƫ�� ��� ��H=
Na2SO4(aq)+H2O(l) ��H=-57.3kJ/mol �¶ȼƺͻ��β�������� ���ձ���û�и�Ӳֽ�����ĭ���ϰ� ƫ�� ��� ��H=![]() kJ/mol 10min��ע���������ƶ��ľ����10min�ڲ������������ bd
kJ/mol 10min��ע���������ƶ��ľ����10min�ڲ������������ bd
��������
(1)��������к��ȵĺ�����д�Ȼ�ѧ����ʽ��
(2)�������к��Ȳⶨʵ��Ĺ��̺����������к���ʵ��ʱ����IJ���������
�ڸ���������װ��ͼ����֪ȱ��Ӳֽ�壬���ձ����粻��Ӳֽ�壬��ʹһ��������ɢʧ��
��ǿ��ǿ���ϡ��Һ�������к��ȵIJⶨ������
�ܸ��ݹ�ʽֱ�������
(3)��Ҫ�ⶨ��Ӧ���ʣ�����Ҫ�ⶨ����һ�������ռ�����������;
�ڸ���Ӱ�췴Ӧ�������غ�ʵ�ʷ����ķ�Ӧ���з�����
(1) �к�����ֵΪ57.3 kJ/mol����Ӧ���ȣ����к��ȵ��Ȼ�ѧ����ʽ��NaOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)+H2O(l) ��H=-57.3kJ/mol���ʴ�Ϊ��NaOH(aq)+
Na2SO4(aq)+H2O(l) ��H=-57.3kJ/mol���ʴ�Ϊ��NaOH(aq)+![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)+H2O(l) ��H=-57.3kJ/mol��
Na2SO4(aq)+H2O(l) ��H=-57.3kJ/mol��
(2) ���������ȼƵĽ����ԭ���������ⶨ�к���ʵ��ʱ����IJ����������ձ�����Ͳ���¶ȼơ����β�����������ʴ�Ϊ���¶ȼơ����β����������
��ʵ��װ�ñ��¡�����Ч������ã�����Ӱ��ʵ����������װ��ȱ��Ӳֽ�����ĭ���ϰ壬�ʴ�Ϊ�����ձ���û�и�Ӳֽ�����ĭ���ϰ壻
��ǿ��ǿ���ϡ��Һ�������к��ȵIJⶨ�����������к�����ȣ��ʴ�Ϊ����ȣ�
���ɹ�ʽ����H=![]() =
=![]() kJ/mol���ʴ�Ϊ����H=
kJ/mol���ʴ�Ϊ����H=![]() kJ/mol��
kJ/mol��
(3)��Ҫ�ⶨ��Ӧ���ʣ�����Ҫ�ⶨ����һ�������ռ��������������ʴ�Ϊ��10min��ע���������ƶ��ľ����10min�ڲ��������������
�������Ӧ���ھ��ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ�������������a. ����Na2CO3��Һ��������̼���Ʒ�Ӧ�����������٣�����b.����K2SO4��Һ�������Ũ�ȼ�С����Ӧ���ʼ�С����ȷ��c.����NaNO3��Һ���������ǿ�����ԣ����ܷų�����������d. ��������ˮ�������Ũ�ȼ�С����Ӧ���ʼ�С����ȷ��e. ����CuSO4��Һ��п��ͭ���ӷ�Ӧ�û���ͭ�����������٣����ʴ�Ϊ��bd��

����Ŀ����ͼ��ʾװ�ü�����ϩʱ����Ҫ���ӵ���

��ϩ���Ʊ� | �Լ�X | �Լ�Y | |
A | CH3CH2Br��NaOH�Ҵ���Һ���� | H2O | KMnO4������Һ |
B | CH3CH2Br��NaOH�Ҵ���Һ���� | H2O | Br2��CCl4��Һ |
C | CH3CH2OH��ŨH2SO4������170�� | NaOH��Һ | KMnO4������Һ |
D | CH3CH2OH��ŨH2SO4������170�� | NaOH��Һ | Br2��CCl4��Һ |